
题目列表(包括答案和解析)
下面的判断中正确的是
A.不用其它试剂只利用液体间的相互混合就能鉴别酒精、四氯化碳、甲苯、溴水和Na2CO3溶液
B.最外层电子数为偶数的短周期元素不会与卤素或氢形成最简式为AB3型的化合物
C.在由水电离提供的C(H+)为10—4mol·L-1的溶液中,Fe3+、SO42-、NO3-、ClO-离子可以大量共存
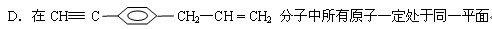
下面的判断中正确的是
A.不用其它试剂只利用液体间的相互混合就能鉴别酒精、四氯化碳、甲苯、溴水和Na2CO3溶液
B.最外层电子数为偶数的短周期元素不会与卤素或氢形成最简式为AB3型的化合物
C.在由水电离提供的C(H+)为10—4mol·L-1的溶液中,Fe3+、SO42-、NO3-、ClO-离子可以大量共存
D.在CH≡C—![]() —CH2—CH = CH2 分子中所有原子一定处于同一平面
—CH2—CH = CH2 分子中所有原子一定处于同一平面
|
下面是某学生利用数据分析的情况,其中不正确的是 | |
| [ ] | |
A. |
根据气体的相对分子质量,可以比较两种气体在同温同压下密度的大小 |
B. |
根据甲烷和乙烷的熔点,可以比较二者晶体中的分子间作用力的大小 |
C. |
根据同周期金属元素原子半径的大小,可以比较同周期元素的金属性强弱 |
D. |
根据液体密度的大小,可以判断液体的挥发性的强弱 |
|
下面是某学生利用数据分析的情况,其中不正确的是 | |
| [ ] | |
A. |
根据气体的相对分子质量,可以比较两种气体在同温同压下密度的大小 |
B. |
根据甲烷和乙烷的熔点,可以比较二者晶体中的分子间作用力的大小 |
C. |
根据同周期金属元素原子半径的大小,可以比较同周期元素的金属性强弱 |
D. |
根据液体密度的大小,可以判断液体的挥发性的强弱 |
CO2是生活中常见的化合物之一,随着世界工业经济的发展、人口的剧增,全球能源紧张及世界气候面临越来越严重的问题,人类对CO2的性质研究和综合利用日益重视。
Ⅰ.在催化剂作用下,可由甲醇和CO2直接合成碳酸二甲酯(DMC):CO2 + 2CH3OH → CO(OCH3)2 + H2O,但甲醇转化率通常不会超过1%,这是制约该反应走向工业化的主要原因。某研究小组在其他条件不变的情况下,通过研究温度、反应时间、催化剂用量分别对转化数(TON)的影响来评价催化剂的催化效果。计算公式为:TON=转化的甲醇的物质的量/催化剂的物质的量。
(1)根据反应温度对TON的影响图(相同时间内测定),判断该反应的焓变△H________0(填“>”、“=”或“<”),理由是____________________________________。

(2)根据反应时间对TON的影响图(上图),已知溶液总体积10mL,反应起始时甲醇0.25mol,催化剂0.6×10—5 mol,计算该温度下,4~7 h内DMC的平均反应速率:________。
(3)根据该研究小组的实验及催化剂用量对TON的影响图(见上右图),判断下列说法正确的是 。
A.由甲醇和CO2直接合成DMC,可以利用甲醇把影响环境的温室气体CO2 转化为资源,在资源循环利用和环境保护方面都具有重要意义
B. 在反应体系中添加合适的脱水剂,将提高该反应的TON
C. 当催化剂用量低于1.2×10—5 mol时,随着催化剂用量的增加,甲醇的平衡转化率显著提高
D. 当催化剂用量高于1.2×10—5 mol时,随着催化剂用量的增加DMC的产率反而急剧下降
Ⅱ.如果人体内的CO2不能顺利排除体外会造成酸中毒,缓冲溶液可以抵御外来少量酸或碱对溶液pH的影响,人体血液里主要通过碳酸氢盐缓冲体系(H2CO3/HCO3-)维持pH稳定。己知正常人体血液在正常体温时,H2CO3的一级电离常数Ka1=10-6.1,c(HCO3-):c(H2CO3)≈20:1,lg2=0.3。
(4)由题给数据可算得正常人体血液的pH________(保留一位小数)。
(5)正常人体血液中H2CO3、HCO3-、OH-、H+四种微粒浓度由大到小关系为: 。
(6)当少量的酸、碱进入血液中时,血液pH变化不大,其原因是 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com