
题目列表(包括答案和解析)
| 浓硫酸 | 170℃ |
| H2SO4(浓) |
| 170℃ |
| 乙醇 | 1,2-二溴乙烷 | 乙醚 | 溴 | |
| 色、态 | 无色液体 | 无色液体 | 无色液体 | 深红棕色液体 |
| 密度/(g?cm-3) | 0.79 | 2.2 | 0.71 | 3.1 |
| 沸点/℃ | 78.5 | 132 | 34.6 | 59.47 |
| 熔点/℃ | -130 | 9 | -116 | -7.25 |
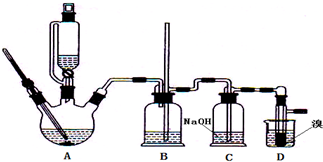
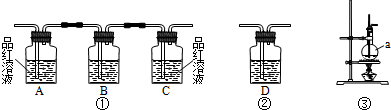
实验室用粗锌与稀硫酸反应制取氢气,利用氢气还原氧化铜来测定铜的相对原子质量。实验装置如下:
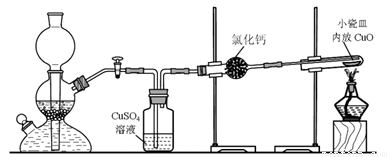
(1)在启普发生器中纯锌与稀硫酸反应过于缓慢,可采取的加快速率的措施是①适当增大硫酸的浓度,②_______________________。
(2)用纯度不高的锌(粗锌)制取氢气,反应速率快,但制得的氢气因含H2S等还原性杂质而有难闻的气味,CuSO4洗气瓶中观察到的现象是_______________,是否可以将CuSO4溶液换成浓硫酸_________(答“是”或“否”) ;理由是__________________________。
(3)有同学发现粗锌与稀硫酸反应一段时间后,锌粒表面变黑,于是收集了少量该黑色固体,验证黑色固体含铁元素的简单化学方法_________________________________________。
(4)实验中得到的数据有:小瓷皿的质量m g,小瓷皿加样品的质量n g,反应后小瓷皿加固体的质量w g,已知氧的相对原子质量为16,则铜的相对原子质量是____________(用含m、n、w的代数式表示)。
(5)某次实验中测定结果明显偏大,可能的原因是________(选填编号)。
a.未充分冷却即停止通氢气 b.氧化铜样品中含有氯化铵杂质
c.反应后固体中有少量Cu2O d.氢气不干燥有少量水分
(6)由于启普发生器药品用量较多,利用下列仪器装配一套有启普发生器功能的简易装置,你选择____________(选填编号) (支撑仪器、橡皮塞、导气管略)。

(a) (b) (c) (d) (e) (f)
实验室用粗锌与稀硫酸反应制取氢气,利用氢气还原氧化铜来测定铜的相对原子质量。实验装置如下:
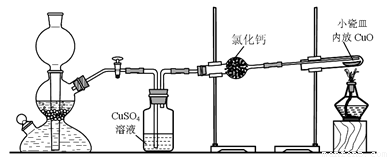
在启普发生器中纯锌与稀硫酸反应过于缓慢,可采取的加快速率的措施是①适当增大硫酸的浓度,②_______________________。
用纯度不高的锌(粗锌)制取氢气,反应速率快,但制得的氢气因含H2S等还原性杂质而有难闻的气味,CuSO4洗气瓶中观察到的现象是_______________,是否可以将CuSO4溶液换成浓硫酸_________(答“是”或“否”) ;理由是__________________________。
有同学发现粗锌与稀硫酸反应一段时间后,锌粒表面变黑,于是收集了少量该黑色固体,验证黑色固体含铁元素的简单化学方法_________________________________________。
实验中得到的数据有:小瓷皿的质量mg,小瓷皿加样品的质量n g,反应后小瓷皿加固体的质量w g,已知氧的相对原子质量为16,则铜的相对原子质量是____________(用含m、n、w的代数式表示)。
某次实验中测定结果明显偏大,可能的原因是________(选填编号)。
a.未充分冷却即停止通氢气 b.氧化铜样品中含有氯化铵杂质
c.反应后固体中有少量Cu2O d.氢气不干燥有少量水分
由于启普发生器药品用量较多,利用下列仪器装配一套有启普发生器功能的简易装置,你选择____________(选填编号) (支撑仪器、橡皮塞、导气管略)。

(a) (b) (c) (d) (e) (f)
实验室用铜和浓硫酸反应制取二氧化硫,下列有关该反应的说法错误的是( )
A.铜是还原剂,发生了氧化反应
B.每生成64 g SO2,转移电子的物质的量是2 mol
C.每消耗1 mol Cu,起氧化剂作用的硫酸消耗2 mol
D.在此反应中,浓硫酸表现出酸性和氧化性
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com