
题目列表(包括答案和解析)
制备氰化钙的化学方程式为
CaCO3 + 2HCN = Ca(CN)2 + CO↑+ H2↑ + CO2↑,在反应中( )
A. 氢元素被氧化,碳元素被还原
B. HCN既是氧化剂又是还原剂
C. Ca(CN)2是氧化产物,H2 是还原产物
D. CO为氧化产物,H2 为还原产物
制备氰化钙的化学方程式为
CaCO3 + 2HCN = Ca(CN)2 + CO↑+ H2↑ + CO2↑,在反应中( )
A. 氢元素被氧化,碳元素被还原
B. HCN既是氧化剂又是还原剂
C. Ca(CN)2是氧化产物,H2 是还原产物
D. CO为氧化产物,H2 为还原产物
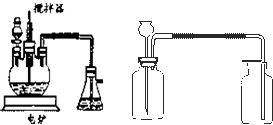 在中学化学实验中,通常用无水硫酸铜检验少量水的存在.由于无水硫酸铜吸湿性很强,需要现制现用.
在中学化学实验中,通常用无水硫酸铜检验少量水的存在.由于无水硫酸铜吸湿性很强,需要现制现用.
| ||
| ||
| ||
| ||


 三聚氰胺(结构简式如右)由于含氮量高而常被不法商人用作食品添加剂,因此三聚氰胺也被人称为“蛋白精”. 三聚氰胺是一种纯白色晶体,无味,常压熔点354℃(分解);快速加热升华,升华温度300℃.三聚氰胺早期合成使用双氰胺法:由电石(CaC2)在N2氛围中加热可制备氰胺化钙(CaCN2),氰胺化钙水解后二聚生成双氰胺(C2H4N4),再加热即转化为三聚氰胺.与该法相比,尿素法成本低,目前较多采用.尿素以氨气为载体,硅胶为催化剂,在380-400℃温度下沸腾反应生成三聚氰胺:6CO(NH2)2→C3N6H6+6NH3+3CO2.
三聚氰胺(结构简式如右)由于含氮量高而常被不法商人用作食品添加剂,因此三聚氰胺也被人称为“蛋白精”. 三聚氰胺是一种纯白色晶体,无味,常压熔点354℃(分解);快速加热升华,升华温度300℃.三聚氰胺早期合成使用双氰胺法:由电石(CaC2)在N2氛围中加热可制备氰胺化钙(CaCN2),氰胺化钙水解后二聚生成双氰胺(C2H4N4),再加热即转化为三聚氰胺.与该法相比,尿素法成本低,目前较多采用.尿素以氨气为载体,硅胶为催化剂,在380-400℃温度下沸腾反应生成三聚氰胺:6CO(NH2)2→C3N6H6+6NH3+3CO2.湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com