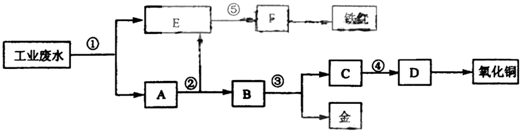
ЃЈ2011?ЫЩНЧјФЃФтЃЉЙЄвЕЩЯВЩгУСђЛЏФЦ-ЪЏЛвЬњбЮЗЈДІРэИпЩщЗЯЫЎЃЈЩщЕФжївЊДцдкаЮЪНЮЊH
3AsO
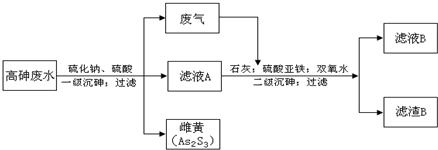
3ЃЉШЁЕУСЫКмКУЕФаЇЙћЃЎЪЕЯжСЫЗЯЫЎДІРэЙ§ГЬЕФЁАШ§ЗЯЁБСуХХЗХЃЎЦфжївЊЙЄвеСїГЬШчЯТЃК
вбжЊЃКЂйбЧЩщЫсЃЈH
3AsO
3ЃЉЛЙдадНЯЧПЃЌвзБЛбѕЛЏЮЊЩщЫсЃЈH
3AsO
4ЃЉ
ЂкбЧЩщЫсбЮЕФШмНтадДѓгкЯргІЕФЩщЫсбЮ[ШчKspЃЈFeAsO
3ЃЉЃОKspЃЈFeAsO
4ЃЉ]
ЧыЛиД№вдЯТЮЪЬтЃК
ЃЈ1ЃЉЗЯЦјЕФжївЊГЩЗжЮЊ
H2S
H2S
ЃЌЭЈЙ§гыЪЏЛвЗЂЩњ
жаКЭЗДгІЃЈЛђИДЗжНтЗДгІЃЉ
жаКЭЗДгІЃЈЛђИДЗжНтЗДгІЃЉ
ЗДгІЃЈЬюЛљБОЗДгІРраЭЃЉБЛЮќЪеЃЎ
ЃЈ2ЃЉаДГівЛМЖГСЩщЙ§ГЬжаЩњГЩДЦЛЦЕФРызгЗНГЬЪНЃК
2H3AsO3+3S2-+6H+=As2S3Ё§+6H2OЃЈЛђ2H3AsO3+3S2-=As2S3Ё§+6OH-ЃЛH++OH-=H2OЃЉ
2H3AsO3+3S2-+6H+=As2S3Ё§+6H2OЃЈЛђ2H3AsO3+3S2-=As2S3Ё§+6OH-ЃЛH++OH-=H2OЃЉ
ЃЎ
ЃЈ3ЃЉТЫвКAжаЃЌГ§СЫгаNa
2SO
4ЁЂH
2SO
4вдЭтЃЌЛЙгаШмжЪ
H3AsO3
H3AsO3
ЃЎ
ЃЈ4ЃЉЖўМЖГСЩщЙ§ГЬжаЪЙгУЫЋбѕЫЎЕФФПЕФга
ABC
ABC
ЃЎ
AЃЎНЋШ§МлЩщбѕЛЏЮЊЮхМлЩщЃЌвдЬсИпГ§ЩщаЇЙћ
BЃЎНЋFe
2+бѕЛЏПЩЩњГЩFeЃЈOHЃЉ
3ГСЕэЃЌвдМгЫйаќИЁЮяЕФГСНЕ
CЃЎзїТЬЩЋбѕЛЏМСЃЌВЛв§НјаТЕФдгжЪ
ЃЈ5ЃЉЙ§ТЫВйзїГЃгУЕФВЃСЇвЧЦїгаЃК
ТЉЖЗЁЂЩеБЁЂВЃСЇАє
ТЉЖЗЁЂЩеБЁЂВЃСЇАє
ЃЈ6ЃЉТЫдќBЕФжївЊГЩЗжга
FeAsO4ЁЂCa3ЃЈAsO4ЃЉ2ЁЂCa3ЃЈAsO3ЃЉ2ЁЂFeЃЈOHЃЉ3ЁЂCaSO4
FeAsO4ЁЂCa3ЃЈAsO4ЃЉ2ЁЂCa3ЃЈAsO3ЃЉ2ЁЂFeЃЈOHЃЉ3ЁЂCaSO4
ЃЈаДСНжжЃЌгУЛЏбЇЪНБэЪОЃЉЃЎ