
题目列表(包括答案和解析)
| 实验步骤 | 实验现象 | 结论 | |
| 方案1 | 取少量氢氧化钠溶液放入试管中,滴入2滴无色酚酞试液 | 无色酚酞试液变红 | 假设一成立 |
| 方案2 | 取少量氢氧化钠溶液放入试管中,滴入过理BaCl2溶液,再滴入无色酚酞试液 | 有白色沉淀产生,酚酞变红 | 假设 |
| 有白色沉淀产生,酚酞不变红 | 假设 |
| 实验步骤 | 实验现象 | 结论 | |
| 方案1 | 取少量氢氧化钠溶液放入试管中,滴入2滴无色酚酞试液 | 无色酚酞试液变红 | 假设一成立 |
| 方案2 | 取少量氢氧化钠溶液放入试管中,滴入过理BaCl2溶液,再滴入无色酚酞试液 | 有白色沉淀产生,酚酞变红 | 假设______成立 |
| 有白色沉淀产生,酚酞不变红 | 假设______成立 |
| ||

| ||
| ||
| ||
| ||
| ||
| ||
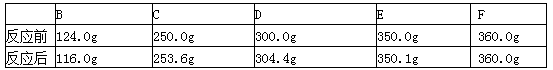
| B | C | D | E | F | |
| 反应前 | 124.0g | 250.0g | 300.0g | 350.0g | 360.0g |
| 反应后 | 116.0g | 253.6g | 304.2g | 350.2g | 360.0g |
 :固体为CuCO3,理由: ① (用化学反应方程式表示)。猜想二:固体为Cu(OH)2,理由:Na2CO3溶液呈碱性。 猜想三:固体为Cu(OH)2和CuCO3的混合物。
:固体为CuCO3,理由: ① (用化学反应方程式表示)。猜想二:固体为Cu(OH)2,理由:Na2CO3溶液呈碱性。 猜想三:固体为Cu(OH)2和CuCO3的混合物。  CuSO4 + 5H2O↑;
CuSO4 + 5H2O↑;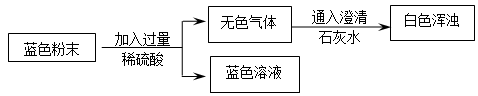
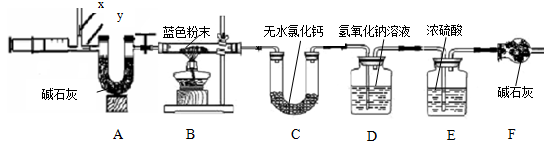
将过量的Na2CO3溶液滴入到一定量CuSO4溶液中得到蓝色固体.某研究性学习小组对固体沉淀的成分进行了如下探究.请完成下列各题:
(一)猜想与假设:
猜想一:固体为CuCO3,理由: (用化学反应方程式表示).
猜想二:固体为Cu(OH)2,理由:Na2CO3溶液呈碱性.
猜想三:固体为Cu(OH)2和CuCO3的混合物.
(二)资料查阅:
①结晶水合物受热后易失去结晶水,如CuSO4•5H2O CuSO4+5H2O↑;
CuSO4+5H2O↑;
②Cu(OH)2、CuCO3受热易分解,各生成对应的两种氧化物.
③无水氯化钙可做吸水剂;碱石灰的主要成分为氢氧化钠固体和氧化钙
(三)设计与实验:
Ⅰ.固体的获取:将反应后的固、液混合物经过滤、洗涤、室温晾干得蓝色固体.
Ⅱ.定性探究固体的成分:
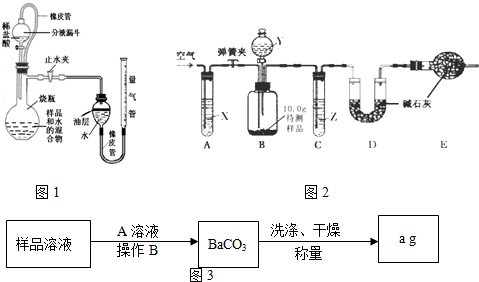
用图1所示方案,进行实验,并得到下列现象:
(1)上图中无色气体为 ,所以猜想二不成立.
(2)向蓝色溶液中加入足量的铁屑,实验现象为 .
发生反应的方程式为 、 .
Ⅲ.定量测定固体的组成:
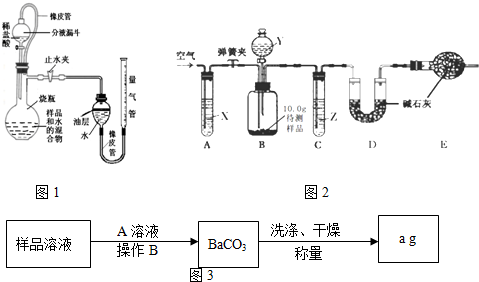
设固体为aCu(OH)2•bCuCO3•cH2O,为测定其组成,称取24.0g蓝色固体.继续进行实验:

图2中注射器处为两个单向阀:推注射器时x关闭,y处打开;拉注射器时,x打开进空气,y关闭.
实验步骤:①组装好装置,检查气密性;②反复推拉注射器;③称量B、C、D、E、F的质量;④关闭弹簧夹,加热B处玻璃管直到反应不再进行;⑤打开弹簧夹,再次反复缓缓推拉注射器;⑥再次称量B、C、D、E、F的质量.
问题探究:
(3)进行步骤⑤的操作中,注射器活塞要缓缓推动的主要目的是 .
数据处理:
(4)某兴趣小组利用上述方法,测得以下数据:(假定每步反应都完全)
| B | C | D | E | F | |
| 反应前 | 124.0g | 250.0g | 300.0g | 350.0g | 360.0g |
| 反应后 | 116.0g | 253.6g | 304.3g | 350.1g | 360.0g |
E装置质量增加的原因是 ;求该固体的化学式中 a:b:c= .
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com