
题目列表(包括答案和解析)
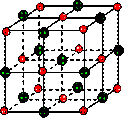
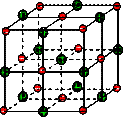
在离子晶体中,阴阳离子按一定规律在空间排列,如图(1)所示即是NaCl的晶体结构,这两种离子在空间三个互相垂直的方向上都是等距离排列的。
①在晶体中,每个Na+离子周围与它最接近的、且距离相等的Cl-共有 个。
每个Na+离子周围与它最接近的、且距离相等的Na+共有 个。而Na+离子数目与Cl-离子数目之比为 。
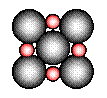
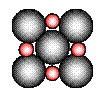
②在离子晶体中,阴阳离子具有球对称的电子云。它们可以被看成是不等径的刚性圆球,并彼此相切(如图⑵所示)。离子键的键长是相邻阴阳离子的半径之和(如图⑶所示),已知a为常数。
![]()
|
a
(1) (2) (3)
③试回答下列问题:
NaCl晶体中离子键的键长为 。Na+离子半径与Cl-离子
半径比r+/r- = 。(已知 √2=1.414 , √3=1.732, √5=2.236)
④NaCl晶体中不存在分子,但在温度达到1413℃时,NaCl晶体形成气体,并以分子形式存在,现有29.25gNaCl晶体,强热使温度达到1450℃,测得气体体积为5.6L(已折算为标准状况),则此时氯化钠气体的分子式为 。
⑤纳米材料的表面原子占总原子数的比例极大,这是它具有许多特殊性质的原因,假设某氯化钠纳米颗粒的大小和形状恰好等于氯化钠晶胞的大小和形状,则这种纳米颗粒的表面原子占总原子数的百分数为 。
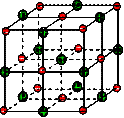
(16分)在离子晶体中,阴阳离子按一定规律在空间排列,如图(1)所示即是NaCl的晶体结构,这两种离子在空间三个互相垂直的方向上都是等距离排列的。 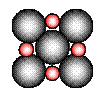
①在晶体中,每个Na+离子周围与它最接近的、且距离相等的Cl-共有 个。
每个Na+离子周围与它最接近的、且距离相等的Na+共有 个。而Na+离子数目与Cl-离子数目之比为 。
②在离子晶体中,阴阳离子具有球对称的电子云。它们可以被看成是不等径的刚性圆球,并彼此相切(如图⑵所示)。离子键的键长是相邻阴阳离子的半径之和(如图⑶所示),已知a为常数。
|

|
Zn和Al都具有两性,其单质和化合物在建筑业、电子工业和石油化工等方面应用广泛。请回答下列问题:
(1) Zn形成金属晶体,其金属原子堆积属于下列 模式
A.简单立方 B.钾型 C.镁型 D.铜型
(2)葡萄糖酸锌[CH2OH(CHOH)4COO]2Zn是目前市场上流行的补锌剂。写出Zn2+基态电子排布式 ; 葡萄糖[CH2OH(CHOH)4CHO]分子中手性碳原子有 个。
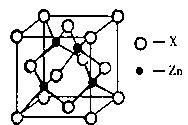
(3)锌与某种元素X通过共价键结合,形成空间网状结构的晶体,下图表示该化合物晶胞,该化合物的化学式为 ;该化合物的晶体熔点远远高于干冰,原因是 。
(4) AlCl3是化工生产中的常用催化剂,熔点为192.6℃,熔融状态以二聚体Al2Cl6形式存在,请问两分子AlCl3之间以 方式二聚。
(选择填写:“离子键”“共价键”“金属键”“氢键”)
(5 )超高导热绝缘耐高温纳米氮化铝(AlN)在绝缘材料中的应用广泛,A1N晶体与金刚石类似,每个Al原子与 个N原子相连,与同一个Al原子相连的N原子构成的空间构型为 。在四大晶体类型中,AlN属于 晶体。
(6)与锌同周期,最外层有3个未成对电子数的元素名称是 ,该元素对应的最低价氢化物分子的中心原子采取了 杂化方式,分子的空间构型是 ,属于 分子(选择填写“极性”“非极性”)。
(12分)Zn和Al都具有两性,其单质和化合物在建筑业、电子工业和石油化工等方面应用广泛。请回答下列问题:
(1) Zn形成金属晶体,其金属原子堆积属于下列 模式
A.简单立方 B.钾型 C.镁型 D.铜型
(2)葡萄糖酸锌[CH2OH(CHOH)4COO]2Zn是目前市场上流行的补锌剂。写出Zn2+基态电子排布式 ; 葡萄糖[CH2OH(CHOH)4CHO]分子中手性碳原子有 个。
(3)锌与某种元素X通过共价键结合,形成空间网状结构的晶体,下图表示该化合物晶胞,该化合物的化学式为 ;该化合物的晶体熔点远远高于干冰,原因是 。
(4) AlCl3是化工生产中的常用催化剂,熔点为192.6℃,熔融状态以二聚体Al2Cl6形式存在,请问两分子AlCl3之间以 方式二聚。
(选择填写:“离子键”“共价键”“金属键”“氢键”)
(5 )超高导热绝缘耐高温纳米氮化铝(AlN)在绝缘材料中的应用广泛,A1N晶体与金刚石类似,每个Al原子与 个N原子相连,与同一个Al原子相连的N原子构成的空间构型为 。在四大晶体类型中,AlN属于 晶体。
(6)与锌同周期,最外层有3个未成对电子数的元素名称是 ,该元素对应的最低价氢化物分子的中心原子采取了 杂化方式,分子的空间构型是 ,属于 分子(选择填写“极性”“非极性”)。

湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com