
题目列表(包括答案和解析)
电石中的碳化钙和水能完全反应,使反应产生的气体排水,测量排出水的体积,可计算出标准状况下乙炔的体积,从而可测定电石中碳化钙的质量分数.
实验室用下图装置进行测定电石中碳化钙质量分数的实验.

(1)如果所制气体流向为从左→右时,装置A、B、C的排列顺序是________,导管口连接顺序是________.
(2)仪器连接好后,进行实验时有下列操作(每项操作只进行一次):
①称取一定量电石,置于装置C中,塞紧橡胶塞;
②检查装置的气密性;
③在装置A和C的分液漏斗中注入适量的水;
④待装置C恢复到室温时,测量装置B中水的体积(导管中存有的水忽略不计);
⑤慢慢开启装置C的分液漏斗的活塞,使水逐滴滴下,至不产生气体时关闭活塞.
正确操作顺序(填写编号)是________.
(3)若实验产生的气体有难闻气味,且测定结果偏大,这是因为气体中含有________杂质.
(4)若实验时称取的电石为1.60g,测量排出水的体积后,折算成标准状况乙炔的体积为448mL,此电石中碳化钙的质量分数为________.
CaC2+2H2O→Ca(OH)2+CH≡CH↑
用反应产生的气体排水,测量排出水的体积,可计算出标准状况下乙炔的体积,从而测定电石中碳化钙的含量。
(1)用下图所列仪器和导管组装实验装置。
序号 | a | b | c |
导管及仪器 |
|
|
|
导管及仪器 |
|
|
|
每个橡皮塞上都打两个孔 | |||
如果所制气体的流向是从左向右的,上述仪器和导管从左到右直接连接的顺序是_______接________接_________接__________接__________接_________。
(2)仪器连接好后,进行实验,有下列操作(每项操作只进行一次)。
①在仪器f中注入适量水。
②称取一定量电石,置于仪器c中,塞紧橡皮塞。
③检查装置的气密性。
④待仪器c恢复到室温时,读取仪器d中水的体积(导管中的水忽略不计)。
⑤慢慢开启仪器f的塞,使水逐滴滴下,直至不产生气体时,关闭活塞。
正确的操作顺序是(填序号)________。
(3)实验中产生的气体常有难闻的气体,这可能是因为制得的乙炔气体中含有H2S、PH3等杂质。这些杂质的存在会使测得结果______。(填“偏大”“偏小”或“没有影响”)
(4)若实验时称取的电石为1.60g,测得排出水的体积,折算成标准状况下,乙炔的体积为448mL,则此电石中碳化钙的质量分数为________。
电石中的碳化钙和水能完全反应:CaC2+2H2O→C2H2↑+Ca(OH)2使反应产生的气体排水,测量排出水的体积,可计算出标准状况乙炔的体积,从而可测定电石中碳化钙的含量.
(1)若用下图仪器和导管组装实验装置:
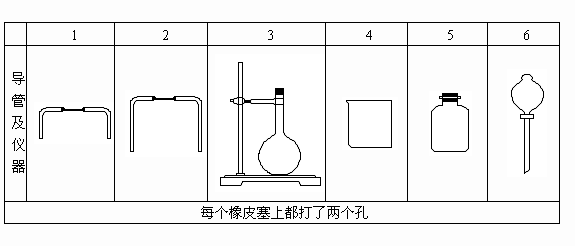
如果所制气体流向从左向右时,上述仪器和导管从左到右直接连接的顺序(填各仪器、导管的序号)是________接________接________接________接________接________.
(2)仪器连接好后,进行实验时,有下列操作(每项操作只进行一次):
①称取一定量电石,置于仪器中,塞紧橡皮塞
②检查装置的气密性
③在仪器6和5中注入适量水
④待仪器3恢复到室温时,量取仪器4中水的体积(导管2中的水忽略不计)
⑤慢慢开启仪器6的活塞,使水逐滴滴下,至不发生气体时,关闭活塞
正确的操作顺序是________(用操作编号填写).
(3)若实验产生的气体有难闻的气味,且测定结果偏大,是因为电石中含有________杂质.
(4)若实验时称取的电石为1.60g,测量排出水的体积后,折算成标准状况乙炔的体积为448ml,此电石中碳化钙的质量分数是________.
电石中的碳化钙和水能完全反应:
CaC2+2H2O→Ca(OH)2+C2H2↑.用反应产生的气体排水,测量排出水的体积,可计算出在标准状况下乙炔的体积,从而可测定电石中碳化钙的含量.(1)用下图所列仪器和导管组装实验装置.如果所制气体流向为从左向右时,下面仪器和导管从左到右直接连接的顺序(填各仪器、导管的序号)是:( )接( )接( )接( )接( )接( );
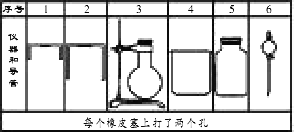
(2)仪器连接好后,进行实验时,有下列操作(每项操作只进行一次):①称取一定质量的电石,置于仪器3中,塞紧橡皮塞;②检查装置的气密性;③在仪器6和5中注入适量水;④待仪器3恢复到室温时,量取仪器4中水的体积(导管2中的水忽略不计);⑤慢慢开启仪器6中的活塞,使水逐渐滴下,至不产生气体时,关闭活塞.正确的操作顺序是________(填编号);
(3)若实验产生的气体有难闻的气味,且测定结果偏大,这是因为电石中含有________杂质;
(4)若实验时称取的电石为1.60 g,测量排出水的体积后,折算成标准状况下乙炔的体积为448 mL,则此电石中CaC2的质量分数为________.
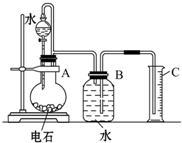 某同学设计了如图所示的实验装置来粗略地测定电石中碳化钙的质量分数.
某同学设计了如图所示的实验装置来粗略地测定电石中碳化钙的质量分数.| 0.29V |
| W |
| 0.29V |
| W |
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com