
题目列表(包括答案和解析)
下图表示各物质之间的转化关系.已知:A、B、I都是XY2型化合物,且阳离子相同,A、B晶体中阴、阳离子个数比都是1∶1,但I晶体中阴、阳离子个数比是2∶1,I常用作干燥剂.
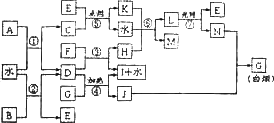
请按要求填空:
(1)I的电子式是________;
(2)反应⑥的化学方程式是________,反应③在工业上的一个重要用途是________;
(3)反应④的化学方程式是________.
(4)已知C的燃料热是1300 kJ·mol-1,表示C的燃烧热的热化学方程式是________.
(5)根据上图中物质之间的转化关系及题中所给信息判断,B的化学式是________.
(12分)、X、Y、Z、W是短周期的四种元素,有关它们的信息如下表所示。
| 元素 | 部分结构知识 | 部分性质 |
| X | X的单质由双原子分子构成,分子中有14个电子 | X有多种氧化物,如XO、XO2、X2O4等;通常情况下XO2与X2O4共存 |
| Y | Y原子的次外层电子数等于最外层电子数的一半 | Y能形成多种气态氧化物 |
| Z | Z原子的最外层电子数多于4 | Z元素的最高正化合价与最低负化合价代数和等于6 |
| W | W原子的最外层电子数等于2n-3(n为原子核外电子层数) | 化学反应中W原子易失去最外层电子形成Wn+ |
(8分) A、B、C、D、E、F六种物质的相互转化关系如下图所示(反应条件未标出),其中反应①是置换反应。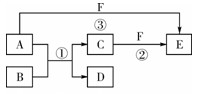
(1)若A是常见的金属单质,D、F是气态单质,反应① 在水溶液中进行,则反应②(在水溶液中进行)的离子方程式是_____________________________。
(2)若B、C、F都是气态单质,且B有毒,③的反应中还有水生成,反应②需要放电才能发生,A、D相遇有白烟生成,则A、D反应产物的电子式是_________________,反应③的化学方程式是______________________________。
(3)若A、D、F都是短周期元素组成的非金属单质,且A、D所含元素同主族,A、F所含元素同周期,则反应①的化学方程式是 。
列举物质B的一个重要用途 。
(8分) A、B、C、D、E、F六种物质的相互转化关系如 下图所示(反应条件未标出),其中反应①是置换反应。
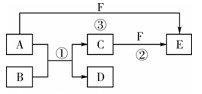
(1)若A是常见的金属单质,D、F是气态单质,反应① 在水溶液中进行,则反应②(在水溶液中进行)的离子方程式是_____________________________。
(2)若B、C、F都是气态单质,且B有毒,③的反应中还有水生成,反应②需要放电才能发生,A、D相遇有白烟生成,则A、D反应产物的电子式是_________________,反应③的化学方程式是______________________________。
(3)若A、D、F都是短周期元素组成的非金属单质,且A、D所含元素同主族,A、F所含元素同周期,则反应①的化学方程式是 。
列举物质B的一个重要用途 。
(12分)、X、Y、Z、W是短周期的四种元素,有关它们的信息如下表所示。
|
元素 |
部分结构知识 |
部分性质 |
|
X |
X的单质由双原子分子构成,分子中有14个电子 |
X有多种氧化物,如XO、XO2、X2O4等;通常情况下XO2与X2O4共存 |
|
Y |
Y原子的次外层电子数等于最外层电子数的一半 |
Y能形成多种气态氧化物 |
|
Z |
Z原子的最外层电子数多于4 |
Z元素的最高正化合价与最低负化合价代数和等于6 |
|
W |
W原子的最外层电子数等于2n-3(n为原子核外电子层数) |
化学反应中W原子易失去最外层电子形成Wn+ |
填写下列空白:(提示:不能用字母X、Y、Z、W作答)
(1)写出X单质的一个重要用途
(2)X、Y、Z三元素的最高价氧化物的水化物酸性由强到弱的顺序是 (填化学式)。
(3)实验室制备X最简单气态氢化物的化学方程式
(4)将少量Y的最高价氧化物通入硅酸钠溶液中反应的离子方程式
(5)W单质与氢氧化钠溶液反应的离子方程式
(6)Z单质在加热的条件下与浓氢氧化钠溶液反应,氧化产物与还原产物的物质的量之
比为1:5则反应的离子方程式
【解析】X的单质由双原子分子构成,分子中有14个电子,所以X的原子序数是7,即为N。次外层电子数等于最外层电子数的一半的原子是C,即Y是C。最高正化合价与最低负化合价代数和等于6,说明Z属于第 ⅦA。因为F没有正价,所以Z是Cl。最外层电子数等于2n-3(n为原子核外电子层数),则n只能是2或3。又因为W原子易失去最外层电子形成Wn+,所以n等于3,即W是Al。在氯气和氢氧化钠的反应中,还原产物是氯离子,若氧化产物和还原产物的物质的量之比是1︰5,则氧化产物中氯元素的化合价是+5价。即为ClO3-。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com