化学在能源开发与利用中起到十分关键的作用.氢气是一种新型的绿色能源,又是一种重要的化工原料.
Ⅰ(1)在298K、101kPa时,2g H
2完全燃烧生成液态水,放出285.8kJ热量.则表示氢气燃烧热的热化学方程式为:______.
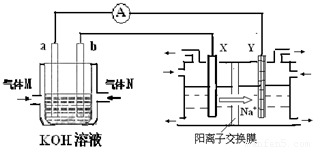
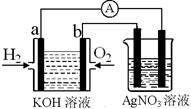
氢氧燃料电池能量转化率高,具有广阔的发展前景.现用氢氧燃料电池进行下图饱和食盐水电解实验(图中所用电极均为惰性电极).分析该装置、回答下列问题:
(2)氢氧燃料电池中,a电极为电池的是______(填“正极”或“负极”),气体M的分子式______,a电极上发生的电极反应式为:______.
(3)若右上图装置中盛有100mL5.0mol/LNaCl溶液,电解一段时间后须加入10.0mol/L盐酸溶液50mL(密度为1.02g/mL)才能使溶液恢复至原来状态.则在此电解过程中导线上转移的电子数为______mol.(保留小数点后2位)
Ⅱ氢气是合成氨的重要原料.工业上合成氨的反应是:
N
2(g)+3H
2(g)?2NH
3 (g)△H=-92.2kJ?mol
-1(4)下列事实中,不能说明上述可逆反应已经达到平衡的是______.
①N
2、H
2、NH
3的体积分数不再改变;
②单位时间内生成2n mol NH
3的同时生成3n mol H
2;
③单位时间内生成3n mol N-H键的同时生成n mol N≡N;
④用N
2、H
2、NH
3的物质的量浓度变化表示的反应速率之比为1:3:2;
⑤混合气体的平均摩尔质量不再改变;
⑥混合气体的总物质的量不再改变.
(5)已知合成氨反应在某温度下2.00L的密闭容器中反应,测得如下数据:
| 物质的量/(mol)/时间(h) | | 1 | 2 | 3 | 4 |
| N2 | 1.50 | n1 | 1.20 | n3 | 1.00 |
| H2 | 4.50 | 4.20 | 3.60 | n4 | 3.00 |
| NH3 | 0.00 | 0.20 | n2 | 1.00 | 1.00 |
根据表中数据计算:
①反应进行到2小时时放出的热量为______kJ.
②0~1小时内N
2的平均反应速率______mol?L
-1?h
-1.
③此条件下该反应的化学平衡常数K═______(保留两位小数).
④反应达到平衡后,若往平衡体系中再加入N
2、H
2 和NH
3各1mol,化学平衡向______方向移动(填“正反应”或“逆反应”或“不移动”.)

 化学在能源开发与利用中起到十分关键的作用.氢气是一种新型的绿色能源,又是一种重要的化工原料.
化学在能源开发与利用中起到十分关键的作用.氢气是一种新型的绿色能源,又是一种重要的化工原料.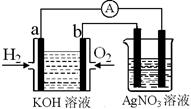
 2H2O
2H2O 2NH3(g) ΔH=-92.20 kJ·mol-1。
2NH3(g) ΔH=-92.20 kJ·mol-1。
 2H2O
2H2O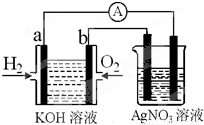
 2H2O
2H2O 2NH3(g) ΔH=-92.20 kJ·mol-1。
2NH3(g) ΔH=-92.20 kJ·mol-1。