
题目列表(包括答案和解析)
北京奥运会“祥云”火炬燃料是丙烷(C3H8),亚特兰大奥运会火炬燃料是丙烯(C3H6)。
(1)丙烷脱氢可得丙烯。
已知:C3H8(g)==== CH4(g)+HC≡CH(g)+H2(g) △H1= +156.6 kJ·mol-1
CH3CH=CH2(g) ====CH4(g)+HC≡CH(g) △H 2= +32.4 kJ·mol-1
则相同条件下,反应C3H8(g)=== CH3CH=CH2(g)+H2(g)的△H = kJ·mol-1。
(2)以丙烷为燃料制作新型燃料电池,其电解质溶液是氢氧化钾溶液。电池正极反应方程式为: ;负极反应方程式: 。
(3)碳氢化合物完全燃烧生成CO2和H2O。常温常压下,空气中的CO2溶于水,得到c(H2CO3)=1.5×10-5 mol·L-1的溶液,测得该溶液的pH=5.60。若忽略水的电离及H2CO3的第二级电离,则H2CO3HCO3-+H+的平衡常数K1= 。(已知
10-5.60=2.5×10-6)
(4)常温下,0.1mol·L-1 NaHCO3溶液的pH大于8,则溶液中c(H2CO3) c(CO32-)(填“>”、“=”或“<”),原因是 (用离子方程式和必要的文字说明)。
北京奥运会“祥云”火炬燃料是丙烷(C3H8),亚特兰大奥运会火炬燃料是丙烯(C3H6)。
(1)丙烷脱氢可得丙烯。
已知:C3H8(g) ==== CH4(g)+HC≡CH(g)+H2(g) △H1= +156.6 kJ·mol-1
CH3CH=CH2(g) ==== CH4(g)+HC≡CH(g) △H 2= +32.4 kJ·mol-1
则相同条件下,反应C3H8(g) === CH3CH=CH2(g)+H2(g)的△H = kJ·mol-1。
(2)以丙烷为燃料制作新型燃料电池,其电解质溶液是氢氧化钾溶液。电池正极反应方程式为: ;负极反应方程式: 。
(3)碳氢化合物完全燃烧生成CO2和H2O。常温常压下,空气中的CO2溶于水,得到c(H2CO3)=1.5×10-5 mol·L-1的溶液,测得该溶液的pH=5.60。若忽略水的电离及H2CO3的第二级电离,则H2CO3 HCO3-+H+的平衡常数K1=
。(已知
HCO3-+H+的平衡常数K1=
。(已知
10-5.60=2.5×10-6)
(4)常温下,0.1 mol·L-1 NaHCO3溶液的pH大于8,则溶液中c(H2CO3) c(CO32-)(填“>”、“=”或“<”),原因是 (用离子方程式和必要的文字说明)。
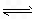 HCO3-+H+的平衡常数K1=________.(已知:10-5.60=2.5×10-6)
HCO3-+H+的平衡常数K1=________.(已知:10-5.60=2.5×10-6) 北京奥运会“祥云”火炬燃料是丙烷(C3H8),亚特兰大奥运会火炬燃料是丙烯(C3H6)。
(1)丙烷脱氢可得丙烯。
已知:C3H8(g) ==== CH4(g)+HC≡CH(g)+H2(g) △H1= +156.6 kJ·mol-1
CH3CH=CH2(g) ==== CH4(g)+HC≡CH(g) △H 2= +32.4 kJ·mol-1
则相同条件下,反应C3H8(g) === CH3CH=CH2(g)+H2(g)的△H = kJ·mol-1。
(2)以丙烷为燃料制作新型燃料电池,其电解质溶液是氢氧化钾溶液。电池正极反应方程式为: ;负极反应方程式: 。
(3)碳氢化合物完全燃烧生成CO2和H2O。常温常压下,空气中的CO2溶于水,得到c(H2CO3)=1.5×10-5 mol·L-1的溶液,测得该溶液的pH=5.60。若忽略水的电离及H2CO3的第二级电离,则H2CO3![]() HCO3-+H+的平衡常数K1= 。(已知
HCO3-+H+的平衡常数K1= 。(已知
10-5.60=2.5×10-6)
(4)常温下,0.1 mol·L-1 NaHCO3溶液的pH大于8,则溶液中c(H2CO3) c(CO32-)(填“>”、“=”或“<”),原因是 (用离子方程式和必要的文字说明)。
北京奥运会“祥云”火炬燃料是丙烷(C3H8),亚特兰大奥运会火炬燃料是丙烯(C3H6).
(1)丙烷脱氢可得丙烯.已知:
C3H8(g)则相同条件下,反应C3H8(g)![]() CH3CH=CH2(g)+H2(g)的ΔH=________kJ·mol-1.
CH3CH=CH2(g)+H2(g)的ΔH=________kJ·mol-1.
(2)以丙烷为燃料制作新型燃料电池,电池的正极通入O2和CO2,负极通入丙烷,电解质是熔融碳酸盐.电池反应方程式为________;放电时,CO32-移向电池的________(填“正”或“负”)极.
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com