
化学在能源开发与利用中起着十分关键的作用.氢气是一种新型的绿色能源,又是一种重要的化工原料.
I.氢氧燃料电池能量转化率高,具有广阔的发展前景.现用氢氧燃料电池进行如图实验(图中所用电极均为惰性电极):
(1)对于氢氧燃料电池中,下列表达不正确的是
CD
CD
A.a电极是负极,OH
-移向负极
B.b电极的电极反应为:O
2+2H
2O+4e
-=4OH
-C.电池总反应式为:2H
2+O
22H
2O
D.电解质溶液的pH保持不变
E.氢氧燃料电池是一种不需要将还原剂和氧化剂全部储藏在电池内的新型发电装置
(2)上图装置中盛有100mL、0.1mol?L
-1AgNO
3溶液,当氢氧燃料电池中消耗氢气112mL(标准状况下)时,则此时上图装置中溶液的pH=
1
1
(溶液体积变化忽略不计)
II氢气是合成氨的重要原料.工业上合成氨的反应是:N
2(g)+3H
2(g)?2NH
3(g)△H=-92.20kJ?mol
-1.
(1)下列事实中,不能说明上述可逆反应已达到平衡的是
②③
②③
(填序号)
①单位时间内生成2n mol NH
3的同时生成3n mol H
2②单位时间内生成n mol N-H的同时生成n mol N≡N
③用N
2、H
2、NH
3的物质的量浓度变化表示的反应速率之比为1:3:2
④N
2、H
2、NH
3的体积分数不再改变
⑤混合气体的平均摩尔质量不再改变
⑥混合气体的总物质的量不再改变
(2)已知合成氨反应在某温度下2L的密闭容器中进行,测得如下数据:
时间(h)
物质的量(mol) |
0 |
1 |
2 |
3 |
4 |
| N2 |
1.50 |
n1 |
1.20 |
n3 |
1.00 |
| H2 |
4.50 |
4.20 |
3.60 |
n4 |
3.00 |
| NH3 |
0 |
0.20 |
N2 |
1.00 |
1.00 |
根据表中数据计算:
①反应进行到2小时时放出的热量为
27.66kJ
27.66kJ
②此条件下该反应的化学平衡常数K=
(保留两位小数)
③反应达到平衡后,若往平衡体系中再加入N
2、H
2和NH
3各1.00mol,化学平衡将向
正反应
正反应
方向移动(填“正反应”或“逆反应”、“不移动”).









 化学在能源开发与利用中起着十分关键的作用.氢气是一种新型的绿色能源,又是一种重要的化工原料.
化学在能源开发与利用中起着十分关键的作用.氢气是一种新型的绿色能源,又是一种重要的化工原料.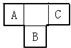 A、B、C、D、E为短周期元素,A、B、C在周期表中所处的位置如图所示,A、C两元素的原子核外电子数之和等于B原子的质子数,B原子核内质子数和中子数相等.D与A同周期,其最高正价与最低负价代数和为零.A、E可形成AE3型分子,分子中只存在极性键.
A、B、C、D、E为短周期元素,A、B、C在周期表中所处的位置如图所示,A、C两元素的原子核外电子数之和等于B原子的质子数,B原子核内质子数和中子数相等.D与A同周期,其最高正价与最低负价代数和为零.A、E可形成AE3型分子,分子中只存在极性键. 


