
题目列表(包括答案和解析)
(12分)在实验室里可用下图所示装置(夹持装置末画出)制取氯酸钾、次氯酸钾和探究氯水的性质。
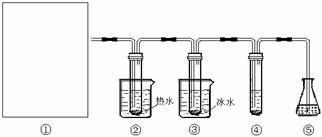
图中:①为氯气发生装置;②试管里盛有15mL 30%KOH溶液,并置于水浴中;③试管里盛有15mL 8% KOH溶液,并置于冰水浴中;④试管里加有紫色石蕊试液;⑤为尾气吸收装置。
请填写下列空白:
(1)在答题卡方框中画出二氧化锰和浓盐酸制取氯气的装置图(铁架台和加热装置可不画出)
(2)制取氯气时,向烧瓶中加入适量浓盐酸的操作是 。
(3)比较制取氯酸钾和次氯酸钾的条件,二者的差异是: 。
![]()
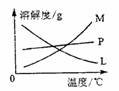 反应完毕经冷却后,②的试管中有大量晶体析出。下图中符合该晶体溶解度曲线的是 (填写编号字母);从②的试管中分离出该晶体的方法是 (填写实验名称)。
反应完毕经冷却后,②的试管中有大量晶体析出。下图中符合该晶体溶解度曲线的是 (填写编号字母);从②的试管中分离出该晶体的方法是 (填写实验名称)。
(4)本实验中制取氯酸钾的离子方程式是 。
(5)实验中可观察到④的试管里溶液的颜色发生了如下变化,请填写下表中的空白:
实验现象 | 原因 |
溶液初从紫色逐渐变为 色 | 氯气与水反应生成的H+使石蕊变色 |
随后溶液逐渐变为无色 |
|
然后溶液从无色逐渐变为 色 |
|
某校化学研究性学习小组的同学在学习了氨的性质持讨论:运用类比的思想,既然氨气具有还原性,能否像H2那样还原CuO呢?他们设计实验制取氨气并探究上述问题.请你参与该小组的活动并完成下列研究:
(一)制取氨气
(1)写出实验制取氨气的化学方程式________;
(2)在实验室中,还可以用浓氨水与________(填写一种试剂)快速制取少量氨气;
(3)有同学模仿排饱和食盐水收集氯气的方法,想用排饱和氯化铵溶液的方法收集氨气.
你认为他能否达到目的?________(填“能”或“否”),理由是____________.
(二)实验探究
该小组中某同学设计了下图所示的实验装置(夹持及尾气处理装置未画出),探究氨气的还原性:

该装置在设计上有一定缺陷,可以采取的的改进措施是__________________.
利用改进后的装置进行实验,观察到CuO变为红色物质,无水CuSO4变蓝色,同时生成一种无污染的N2.
(三)问题讨论
(1)有同学认为:NH3与CuO反应生成的红色物质中可能含有Cu2O.已知:Cu2O是一种碱性氧化物;在酸性溶液中,Cu+的稳定性比Cu2+差(Cu+→Cu+Cu2+).请你设计一个简单的实验检验该红色物质中是否含有Cu2O.________;
(2)在解决了问题(1)后,又有同学提出:Cu2O与CuO的热稳定性哪个更强?于是
他们进行了如下实验:取98 g Cu(OH)2固体,加热至80℃~100℃时,得到黑色固体粉末,继续加热到1 000℃以上,黑色粉末全部变为红色粉末A.冷却后称量,A的质量为72 g.据此可推得,A的化学式为________.由此,得到的结论是________.
(四)兴趣探究
将铜丝的一端绕成螺旋状,在酒精灯外焰加热,冷却后变黑.再在酒精灯上将该铜丝加热至红热状态.如下图所示,趁热插入到试管里的氯化铵晶体中,在试管中出现白烟.冷却后取出铜丝变成亮红色.

(1)试管中出现白烟的有关化学方程式为____________.
(2)铜丝灼热后在氯化铵中由黑变红的有关化学方程式___________.
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com