用18mol?L
-1 浓硫酸配制100mL 3.0mol?L
-1 稀硫酸的实验步骤如下:
①计算所用浓硫酸的体积 ②量取一定体积的浓硫酸 ③溶解 ④转移、洗涤 ⑤定容、摇匀
完成下列问题:
(1)所需浓硫酸的体积是
16.7mL
16.7mL
,量取浓硫酸所用的量筒的规格是
B
B
(从下列中选用
A.10mL B.25mL C.50mL D.100mL).
(2)第③步实验的操作是
把浓硫酸沿烧杯壁缓慢倒入盛水的烧杯中,不断用玻璃棒搅拌散热
把浓硫酸沿烧杯壁缓慢倒入盛水的烧杯中,不断用玻璃棒搅拌散热
(具体操作方法).
(3)第⑤步实验的操作是
继续向容量瓶加水至液面距离刻度线1~2cm时,改用胶头滴管滴加至溶液凹液面与刻度线水平相切,盖好瓶塞颠倒摇匀
继续向容量瓶加水至液面距离刻度线1~2cm时,改用胶头滴管滴加至溶液凹液面与刻度线水平相切,盖好瓶塞颠倒摇匀
(具体操作方法).
(4)第④步实验操作的目的是
尽可能将溶质全部移入容量瓶中
尽可能将溶质全部移入容量瓶中
.
(5)溶液转移到容量瓶之前需要恢复到室温是因为
影响溶液体积,易造成容量瓶炸裂
影响溶液体积,易造成容量瓶炸裂
.
(6)下列情况对所配制的稀硫酸浓度有何影响?(用“偏大”“偏小”“无影响”填写)?
A.所用的浓硫酸长时间放置在密封不好的容器中
偏小
偏小
B.容量瓶用蒸馏洗涤后残留有少量的水
无影响
无影响
C.所用过的烧杯、玻璃棒未洗涤
偏小
偏小
?
D.定容时俯视刻度线
偏大
偏大
?
E.定容时加蒸馏水不慎超过了刻度
偏小
偏小
?

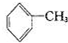 +6KMnO4+9H2SO4=3K2SO4+6MnSO4+14H2O+( )下列说法不正确的是( )
+6KMnO4+9H2SO4=3K2SO4+6MnSO4+14H2O+( )下列说法不正确的是( )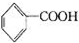
 作氧化剂
作氧化剂