
题目列表(包括答案和解析)
用![]() 和硫粉在水溶液中加热反应,可制得
和硫粉在水溶液中加热反应,可制得![]() .10℃和70℃时,
.10℃和70℃时,![]() 在100g水中的溶解度分别为60.0g和212g.常温下,从溶液中析出的晶体是
在100g水中的溶解度分别为60.0g和212g.常温下,从溶液中析出的晶体是![]() ·5
·5![]() .
.![]() 在酸性溶液中立即完全分解:
在酸性溶液中立即完全分解:
现取15.1g![]() ,溶于80.0mL水.另取5.00g硫粉,用少许乙醇润湿后(以便硫能被水浸润),加到上述溶液中.用小火加热至微沸,反应约1小时后过滤.滤液在100℃经蒸发、浓缩,冷却至10℃后析出
,溶于80.0mL水.另取5.00g硫粉,用少许乙醇润湿后(以便硫能被水浸润),加到上述溶液中.用小火加热至微沸,反应约1小时后过滤.滤液在100℃经蒸发、浓缩,冷却至10℃后析出![]() ·5
·5![]() 晶体.
晶体.
(1)若加入的硫粉不用乙醇润湿,对反应的影响是________.(填写选项的字母)
[ ]
(2)反应1小时后过滤,其目的是________.
(3)滤液中除![]() 和可能未反应完全的亚硫酸钠外,最可能存在的无机杂质是________.它是由________而产生的.如果滤液中该杂质的含量不很低,其检测的方法是:________.
和可能未反应完全的亚硫酸钠外,最可能存在的无机杂质是________.它是由________而产生的.如果滤液中该杂质的含量不很低,其检测的方法是:________.
(4)设![]() 跟硫粉完全反应,当将滤液蒸发浓缩后,冷却至70℃,溶液的体积约30mL,该溶液是否达到饱和?试通过计算说明.(70℃时,
跟硫粉完全反应,当将滤液蒸发浓缩后,冷却至70℃,溶液的体积约30mL,该溶液是否达到饱和?试通过计算说明.(70℃时,![]() 饱和溶液的密度为1.17
饱和溶液的密度为1.17![]() ).
).
(5)若要计算在100℃下将溶液蒸发至体积为30.0mL,再冷却至10℃时所能得到的![]() ·5
·5![]() 的质量,你认为________.(填写一个选项的字母)
的质量,你认为________.(填写一个选项的字母)
[ ]
A.前面提供的数据已经足够
B.还需要提供100℃时溶液的密度(1.14![]() )
)
C.还需要提供结晶后剩余溶液的体积(10.0mL)
(6)根据第(5)小题你的选择(如选(A)则直接计算,如选(B)或(C)则可选用其数据),计算从10℃,30.0mL溶液中结晶而出的![]() ·5
·5![]() 的质量.
的质量.
用![]() 和硫粉在水溶液中进行热反应,可以制得
和硫粉在水溶液中进行热反应,可以制得![]() .10℃和70℃时,
.10℃和70℃时,![]() 在100g水中的溶解度分别为60.0g和212g.常温下,从溶液中析出的晶体是
在100g水中的溶解度分别为60.0g和212g.常温下,从溶液中析出的晶体是![]() ,俗称海波.
,俗称海波.![]() 在酸性溶液中立即完全分解:
在酸性溶液中立即完全分解:
![]()
现取15.1g![]() ,溶于80.0mL水.另取5.00g硫粉,用少量乙醇润湿后(以便硫粉被水浸润),加到上述溶液中.用小火加热至微沸,反应约1小时后过滤.滤液在100℃经蒸发、浓缩、冷却至10℃,析出
,溶于80.0mL水.另取5.00g硫粉,用少量乙醇润湿后(以便硫粉被水浸润),加到上述溶液中.用小火加热至微沸,反应约1小时后过滤.滤液在100℃经蒸发、浓缩、冷却至10℃,析出![]() 晶体.
晶体.
(1)若加入的硫粉不用乙醇润湿,对反应的影响是________.(填写选项字母)
[ ]
|
A.会降低反应速率 |
B.需要提高反应温度 |
|
C.将增大反应体系的pH值 |
D.会减少产量 |
(2)反应1小时后过滤.其目的是________.
(3)滤液中除![]() 和可能未反应完全的
和可能未反应完全的![]() 外,最可能存在的无机杂质是________.它是由________而产生的.如果滤液中该杂质的含量不很低,其检测的方法是________.
外,最可能存在的无机杂质是________.它是由________而产生的.如果滤液中该杂质的含量不很低,其检测的方法是________.
(4)设![]() 跟硫粉反应完全,当将滤液蒸发浓缩后,冷却至70℃,溶液的体积约30mL,该溶液是否达到饱和?试通过计算说明.(70℃时
跟硫粉反应完全,当将滤液蒸发浓缩后,冷却至70℃,溶液的体积约30mL,该溶液是否达到饱和?试通过计算说明.(70℃时![]() 饱和溶液的密度为1.17g/cm3)
饱和溶液的密度为1.17g/cm3)
(5)若要计算在100℃下将溶液蒸发至体积为300mL,再冷却至10℃时所能得到的![]() 的质量,你认为________(填写一个选项字母)
的质量,你认为________(填写一个选项字母)
[ ]
A.前面提供的数据已经足够.
B.还需要提供100℃时溶液的密度.
C.还需要提供结晶后剩余溶液的体积.
沉淀溶解平衡也有平衡常数,称为溶度积常数,符号为Ksp,对于某沉淀溶解平衡:
MmAn(s)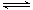 mMn+(aq) + nAm-(aq),Ksp=[c(Mn+)]m·[c(Am-)]n。
mMn+(aq) + nAm-(aq),Ksp=[c(Mn+)]m·[c(Am-)]n。
(1)常温时,Fe(OH)3的Ksp=1×10-38,要使溶液中的Fe3+沉淀完全(残留在溶液中的c(Fe3+)<10-5 mol·L-1),则溶液的pH最小为 。
(2)某温度时,在100g水中溶解0.74g Ca(OH)2达到饱和,此时溶液的体积约为100 mL,则该温度下Ca(OH)2的溶度积常数Ksp= 。(写出计算过程)
t℃时,往100g水中加入w1 g无水硫酸锌或加入w2 g皓矾(ZnSO4·7H2O)晶体,都可使溶液达到饱和状态,则w1和w2的关系符合
[ ]
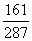 w2
w2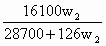
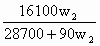
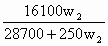
200C时,在100g水中溶解11.1g K2SO4 恰好达到饱和,此饱和溶液的密度为1.08 g/cm3。将350mL此温度的K2SO4 饱和溶液用水稀释至500mL。计算稀释后溶液中K2SO4 的物质的量浓度。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com