
题目列表(包括答案和解析)
| ||
| ||
(08浙江舟山中学月考) 将化学知识的系统化,有助于对化学问题的进一步认识。请你参与。
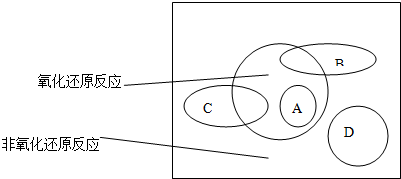
问题1:从不同的角度,化学反应可以有不同的分类方法。四种基本反应类型是从物质的组成和性质进行的分类,氧化还原反应和离子反应则是从其他不同的角度进行分类的。请在右图的方框中,用图示的方法表示离子反应、化合反应和氧化还原反应之间的关系(用一个圆圈表示一类反应)。
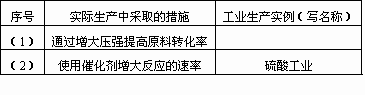
问题2:不同化学反应进行的快慢和程度千差万别。反应的快慢和程度是化工生产考虑的两个重要因素。请你按照表中要求完成下表(填写内容不能重复)。
序号 | 实际生产中采取的措施 | 工业生产实例(写名称) |
(1) | 通过增大压强提高原料转化率 |
|
(2) | 使用催化剂增大反应的速率 |
|
问题3:化学反应中均伴随着能量的变化。如果一个化学反应中,反应物的总能量和生成物的总能量有如图所示的关系,则该反应过程中的能量变化是 (填放热或吸热)。
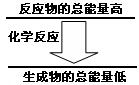
已知热化学方程式为:
C(s) + O2(g)= CO2 (g) △H= ―393.5KJ?mol-1
H2 (g) + 1/2O2 (g)= H2O (l) △H= ―285.8KJ?mol-1
试通过计算说明等质量的氢气和碳燃烧时产生热量的比是 :1(保留1位小数)。
问题4:化学反应的发生是有条件的。反应物相同,反应的条件不同,反应的原理不同。如:
4Na+O2=2Na2O 2Na+O2![]() Na2O2 ;事实上还有许多条件可以影响化学反应的发生,请用化学反应方程式表示下列观点:反应物相同,反应物的浓度不同,反应的原理不同:
Na2O2 ;事实上还有许多条件可以影响化学反应的发生,请用化学反应方程式表示下列观点:反应物相同,反应物的浓度不同,反应的原理不同:
将化学知识的系统化,有助于对化学问题的进一步认识。请你参与下列关于化学反应的讨论。
问题1:从不同的角度,化学反应可以有不同的分类方法。四种基本反应类型是从物质的组成和性质进行的分类,氧化还原反应和离子反应则是从其他不同的角度进行分类的。请在上图的方框中,用图示的方法表示离子反应、化合反应和氧化还原反应之间的关系。
问题2:不同化学反应进行的快慢和程度千差万别。反应的快慢和程度是化工生产考虑的两个重要因素。请你按照表中要求完成下表(填写内容不能重复)。
| 序号 | 实际生产中采取的措施 | 工业生产实例(写名称) |
| (1) | 通过增大压强提高原料转化率 | |
| (2) | 使用催化剂增大反应的速率 |
问题3:化学反应中均伴随着能量的变化。如果一个化学反应中,反应物的总能量和生成物
的总能量有如图所示的关系,则该反应过程中的能量变化是 。
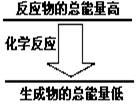 已知热化学方程式为:
已知热化学方程式为:
C(g) + O2(g)= CO2 (g) △H= ―393.5KJ/mol
H2 (g) + 1/2O2 (g)= H2O (l) △H= ―285.8KJ/mol
试通过计算说明等质量的氢气和碳燃烧时产生热量的比是 (保留1位小数)。
问题4:化学反应的发生是有条件的。反应物相同,反应的条件不同,反应的原理不同。
如:4Na+O2=2Na2O 2Na+O2![]() Na2O2 ;事实上还有许多条件可以影响化学反应的发生,请用离子反应方程式表示下列观点:反应物相同,反应物的浓度不同,反应的原理不同: 。
Na2O2 ;事实上还有许多条件可以影响化学反应的发生,请用离子反应方程式表示下列观点:反应物相同,反应物的浓度不同,反应的原理不同: 。
将化学知识的系统化,有助于对化学问题的进一步认识.请你参与下列关于化学反应的讨论.

问题1:从不同的角度,化学反应可以有不同的分类方法.四种基本反应类型是从物质的组成和性质进行的分类,氧化还原反应和离子反应则是从其他不同的角度进行分类的.请在上图的方框中,用图示的方法表示离子反应、化合反应和氧化还原反应之间的关系.
问题2:不同化学反应进行的快慢和程度千差万别.反应的快慢和程度是化工生产考虑的两个重要因素.请你按照表中要求完成下表(填写内容不能重复).

问题3:化学反应中均伴随着能量的变化.如果一个化学反应中,反应物的总能量和生成物的总能量有如图所示的关系,则该反应过程中的能量变化是________.
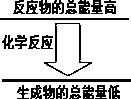
已知热化学方程式为:
C(g)+O2(g)=CO2(g) △H=—393.5KJ/mol
H2(g)+1/2O2(g)=H2O(l) △H=—285.8KJ/mol
试通过计算说明等质量的氢气和碳燃烧时产生热量的比是________(保留1位小数).
问题4:化学反应的发生是有条件的.反应物相同,反应的条件不同,反应的原理不同.如:4Na+O2=2Na2O 2Na+O2![]() Na2O2;事实上还有许多条件可以影响化学反应的发生,请用离子反应方程式表示下列观点:反应物相同,反应物的浓度不同,反应的原理不同:________.
Na2O2;事实上还有许多条件可以影响化学反应的发生,请用离子反应方程式表示下列观点:反应物相同,反应物的浓度不同,反应的原理不同:________.
将化学知识的系统化,有助于对化学问题的进一步认识.请你参与下列关于化学反应的讨论.
问题1:从不同的角度,化学反应可以有不同的分类方法.四种基本反应类型是从物质的组成和性质进行的分类,氧化还原反应和离子反应则是从其他不同的角度进行分类的.请在右图的方框中,用图示的方法表示离子反应、化合反应和氧化还原反应之间的关系.

问题2:不同化学反应进行的快慢和程度千差万别.反应的快慢和程度是化工生产考虑的两个重要因素.请你按照表中要求完成下表(填写内容不能重复).
问题3:化学反应中均伴随着能量的变化.如果一个化学反应中,反应物的总能量和生成物的总能量有如图所示的关系,则该反应过程中的能量变化是________.
已知热化学方程式为:

C(g)+O2(g)=CO2(g)△H=—393.5KJ/mol
H2(g)+1/2O2(g)=H2O(l)△H=—285.8KJ/mol
试通过计算说明等质量的氢气和碳燃烧时产生热量的比是________(保留1位小数).
问题4:化学反应的发生是有条件的.反应物相同,反应的条件不同,反应的原理不同.如:4Na+O2=2Na2O2Na+O2![]() Na2O2;事实上还有许多条件可以影响化学反应的发生,请用离子反应方程式表示下列观点:反应物相同,反应物的浓度不同,
Na2O2;事实上还有许多条件可以影响化学反应的发生,请用离子反应方程式表示下列观点:反应物相同,反应物的浓度不同,
反应的原理不同:________.
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com