
题目列表(包括答案和解析)
(1)提出假设:该反应的气体产物全部是二氧化碳。
(2)设计方案:将一定量的氧化铁在隔绝氧气条件下与过量炭粉完全反应(如下图),测定参加反应的碳元素与氧元素的质量比。
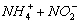
(3)查阅资料:氮气不与碳、氧化铁发生反应,可用来隔绝氧气。实验室可以用氯化铵饱和溶液和亚硝酸钠饱和溶液混合加热反应制得氮气。请写出反应的离子方程式:_____________
_____________________________________________________________________。
(4)实验操作:
操作步骤及实验现象 | 简 答 |
①称取 | — |
②加热前,先通一段时间纯净、干燥的氮气 | 其目的是_____________________________ |
③夹紧T处弹簧夹,加热一段时间,澄清石灰水变浑浊 | 该现象说明___________________________ |
④完全反应后,冷却至室温,称得玻璃管和固体的总质量为 | — |
(5)数据处理:经计算,参加反应的碳元素质量为
(6)得到结论:根据数据处理结果,得出原假设不成立,理由是___________________________。
(7)根据数据处理结果,反应生成的气体是__________,且气体的物质的量之比是__________,该实验的化学方程式为_______________________________________________。
(1)提出假设:该反应的气体产物全部是二氧化碳。
(2)设计方案:将一定量的氧化铁在隔绝氧气条件下与过量炭粉完全反应(如下图),测定参加反应的碳元素与氧元素的质量比。
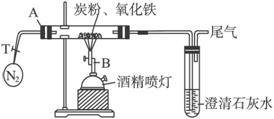
(3)查阅资料:氮气不与碳、氧化铁发生反应,可采用隔绝氧气。实验室可以用氯化铵饱和溶液和亚硝酸钠饱和溶液混合加热反应制得氮气。请写出该反应的离子方程式:
___________________________。
(4)实验操作:
操作步骤及实验现象 | 简答 |
称取 | — |
②加热前,先通一段时间纯净、干燥的氮气 | 其目的是:_________________ |
③夹紧T处弹簧夹,加热一段时间,澄清石灰水变浑浊 | 该现象说明:_________________ |
④完全反应后,冷却至室温,称得玻璃管和固体的总质量为 | — |
(5)数据处理:经计算,参加反应的碳元素质量为
(6)得到结论:根据数据处理结果,得出原假设不成立,理由是:__________________________。
(7)根据数据处理结果,反应生成的气体是_________,且气体的物质的量之比是_________,该实验的化学方程式为:___________________________。
某学生研究性学习小组对过量炭粉与氧化铁反应产物中气体的成分进行研究。
(1)提出假设:该反应的气体产物全部是二氧化碳。
(2)设计方案:将一定量的氧化铁在隔绝氧气条件下与过量炭粉完全反应(如下图),测定参加反应的碳元素与氧元素的质量比。
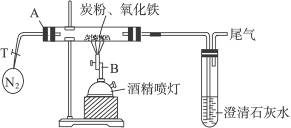
(3)查阅资料:氮气不与碳、氧化铁发生反应,可用来隔绝氧气。实验室可以用氯化铵饱和溶液和亚硝酸钠饱和溶液混合加热反应制得氮气。请写出反应的离子方程式:_____________
______________________________________________________________________________。
(4)实验操作:
| 操作步骤及实验现象 | 简 答 |
| ①称取3.2 g氧化铁与2 g炭粉均匀混合,放入48.48 g的玻璃管中,按上图装置连接 | — |
| ②加热前,先通一段时间纯净、干燥的氮气 | 其目的是_____________________________ |
| ③夹紧T处弹簧夹,加热一段时间,澄清石灰水变浑浊 | 该现象说明___________________________ |
| ④完全反应后,冷却至室温,称得玻璃管和固体的总质量为52.24 g | — |
(5)数据处理:经计算,参加反应的碳元素质量为0.48 g,氧元素质量为0.96 g。
(6)得到结论:根据数据处理结果,得出原假设不成立,理由是___________________________。
(7)根据数据处理结果,反应生成的气体是__________,且气体的物质的量之比是__________,该实验的化学方程式为___________________________________________________________。
(1)假设:该反应的气体产物全部是CO2。
(2)设计方案:将一定量Fe2O3在隔绝氧气的条件下与过量的炭粉完全反应,测定参加反应的碳元素与氧元素的质量,计算出反应产物中碳、氧原子的物质的量比。
(3)查阅资料:N2不与碳、Fe2O3发生反应。实验室可以用氯化铵溶液和亚硝酸钠溶液混合加热制得N2。
①写出实验室制取N2的离子方程式__________________________________________。
②该实验装置与实验室制取下列气体的装置相同的是________________(填标号)。
a.用稀盐酸与锌反应制H2
b.用MnO2与浓盐酸共热制Cl2
c.用NH4Cl与Ca(OH)2共热制NH3
其主要玻璃仪器除酒精灯外,还包括______________、______________。
(4)实验操作步骤、现象:
①实验前要____________________________。
②称取
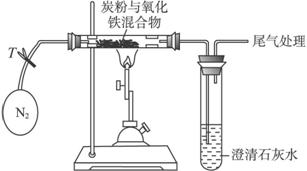
③加热前,先进行的操作是______________,其目的是______________。
④夹紧T处弹簧夹,加热一段时间,证明有CO2气体生成的现象是______________。
⑤反应完全后,冷却至室温,称得玻璃管和固体的总质量为
(5)数据处理:经计算,参加反应的碳元素质量为
(6)结论:根据数据处理结果,得出原假设不成立,理由是______________。
(7)根据数据处理结果,反应生成的气体是______________,且气体的物质的量之比为______________。试写出该反应的化学方程式____________________________。
(1)假设:该反应的气体产物全部是CO2。
(2)设计方案:将一定量Fe2O3在隔绝氧气的条件下与过量的炭粉完全反应,测定参加反应的碳元素与氧元素的质量,计算出反应产物中碳、氧原子的物质的量比。
(3)查阅资料:N2不与碳、Fe2O3发生反应。实验室可以用氯化铵溶液和亚硝酸钠溶液混合加热制得N2。
①写出实验室制取N2的离子方程式______________________________。
②该实验装置与实验室制取下列气体的装置相同的是_______________(填标号)。
a.用稀盐酸与锌反应制H2
b.用MnO2与浓盐酸共热制Cl2
c.用NH4Cl与Ca(OH)2共热制NH3
其主要玻璃仪器除酒精灯外,还包括_______________、_______________。
(4)实验操作步骤、现象:
①实验前要______________________________。
②称取
③加热前,先进行的操作是_______________,其目的是_______________。
④夹紧T处弹簧夹,加热一段时间,证明有CO2气体生成的现象是_______________。
⑤反应完全后,冷却至室温,称得玻璃管和固体的总质量为
(5)数据处理:经计算,参加反应的碳元素质量为
(6)结论:根据数据处理结果,得出原假设不成立,理由是__________________。
(7)根据数据处理结果,反应生成的气体是_______________,且气体的物质的量之比为_______________。试写出该反应的化学方程式_______________。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com