
题目列表(包括答案和解析)
| 沉淀物 | Fe(OH)2 | Zn(OH)2 | Hg(OH)2 |
| 沉淀完全的pH | 9.7 | 8.0 | 5.3 |
| 沉淀物 | FeS | ZnS | HgS |
| 沉淀完全的pH | ≥4.92 | ≥2.72 | ≥2.5 |
| KSP | 3.7×10-19 | 1.2×10-23 | 4×10-53 |
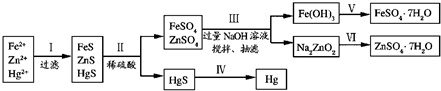
下面能够构成原电池及电极反应式正确的是
A.Fe、Cu、浓硝酸溶液,负极反应式为:Fe-2e- ![]() Fe2+
Fe2+
B.Al、Cu、稀硫酸,负极反应式为:Cu-2e- ![]() Cu2+
Cu2+
C.Al、Mg、NaOH溶液,负极反应式为:Al+4OH--3e- ![]() AlO2-+2H2O
AlO2-+2H2O
D.Zn、Cu、乙醇,负极反应式为:Zn-2e- ![]() Zn2+
Zn2+
| ||
| ||
| ||
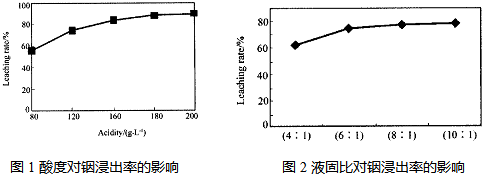

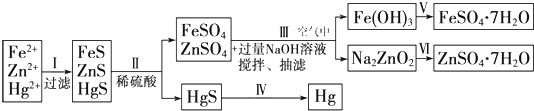
2- 2 |
| 沉淀物 | Fe(OH)2 | Zn(OH)2 | Hg(OH)2 |
| 沉淀完全的pH | 9.7 | 8.0 | 5.3 |
| 沉淀物 | FeS | ZnS | HgS |
| 沉淀完全的pH | ≥4.92 | ≥2.72 | ≥2.5 |
| KSP | 3.7×10-19 | 1.2×10-23 | 4×10-53 |

湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com