
题目列表(包括答案和解析)
右图为农夫山泉矿泉水瓶上的部分说明文字,列出了该饮用天然水理化指标。这里的钙、镁、钾、钠是指
|
饮用天然水理化指标 矿物元素 测定结果 钙≥4.0 mg/L 镁≥0.5 mg/L 钾≥0.35 mg/L 钠≥0.8 mg/L 偏硅酸≥1.8 mg/L pH (25℃) 7.1
【答案】D 【解析】略 【题型】选择题 【适用】较易 【标题】2010年湖南浏阳一中高一上学期期中考试化学试卷 【关键字标签】农夫山泉,指标 【结束】 3【题文】下列实验操作中,错误的是
【答案】D 【解析】略 【题型】选择题 【适用】较易 【标题】2010年湖南浏阳一中高一上学期期中考试化学试卷 【关键字标签】实验操作 【结束】 4【题文】下列说法中正确的是
【答案】B 【解析】略 【题型】选择题 【适用】较易 【标题】2010年湖南浏阳一中高一上学期期中考试化学试卷 【关键字标签】分子数,原子数 【结束】 5【题文】下列有关0.2mol·L-1 BaCl2溶液的说法不正确的是
【答案】A 【解析】略 【题型】选择题 【适用】较易 【标题】2010年湖南浏阳一中高一上学期期中考试化学试卷 【关键字标签】溶液,离子浓度 【结束】 6【题文】下列离子方程式中书写正确的是( )
【答案】B 【解析】略 【题型】选择题 【适用】较易 【标题】2010年湖南浏阳一中高一上学期期中考试化学试卷 【关键字标签】离子方程式,氢氧化钡 【结束】 7【题文】已知有如下反应:①2Fe3++2I-===2Fe2++I2 ②2Fe2++Br2===2Fe3++2Br- ③2Fe(CN)+I2===2Fe(CN)+2I-,试判断氧化性强弱顺序正确的是
【答案】C 【解析】略 【题型】选择题 【适用】较易 【标题】2010年湖南浏阳一中高一上学期期中考试化学试卷 【关键字标签】氧化性,顺序 【结束】 8【题文】实验室制取少量N2常利用的反应是NaNO2+NH4ClNaCl+N2↑+2H2O,关于该反应的说法正确的是
【答案】A 【解析】略 【题型】选择题 【适用】较易 【标题】2010年湖南浏阳一中高一上学期期中考试化学试卷 【关键字标签】实验室,氧化剂 【结束】 9【题文】用托盘天平称量固体物质时,若将样品和砝码放在托盘上的位置颠倒,平衡时托盘上的砝码质量为10g,游码为0.5g,则样品的质量为
【答案】D 【解析】略 【题型】选择题 【适用】较易 【标题】2010年湖南浏阳一中高一上学期期中考试化学试卷 【关键字标签】托盘天平,砝码 【结束】 10【题文】将26克含有SiO2和CaCO3固体在高温下加热至质量不再改变,冷却后称重为17.2克。(已知:SiO2 + CaCO3 CaSiO3 + CO2↑,SiO2和CaSiO3均为固体) (1)求生成的CO2的体积(标准状况下) (2)求原混合物中所含SiO2的质量。 【答案】(1)4.48L (2)6克 【解析】略 【题型】计算题 【适用】较易 【标题】2010年湖南浏阳一中高一上学期期中考试化学试卷 【关键字标签】高温,体积 【结束】 |
右图为农夫山泉矿泉水瓶上的部分说明文字,列出了该饮用天然水理化指标。这里的钙、镁、钾、钠是指
|
饮用天然水理化指标 矿物元素 测定结果 钙≥4.0 mg/L 镁≥0.5 mg/L 钾≥0.35 mg/L 钠≥0.8 mg/L 偏硅酸≥1.8 mg/L pH (25℃) 7.1
【答案】D 【解析】略 【题型】选择题 【适用】较易 【标题】2010年湖南浏阳一中高一上学期期中考试化学试卷 【关键字标签】农夫山泉,指标 【结束】 3【题文】下列实验操作中,错误的是
【答案】D 【解析】略 【题型】选择题 【适用】较易 【标题】2010年湖南浏阳一中高一上学期期中考试化学试卷 【关键字标签】实验操作 【结束】 4【题文】下列说法中正确的是
【答案】B 【解析】略 【题型】选择题 【适用】较易 【标题】2010年湖南浏阳一中高一上学期期中考试化学试卷 【关键字标签】分子数,原子数 【结束】 5【题文】下列有关0.2mol·L-1 BaCl2溶液的说法不正确的是
【答案】A 【解析】略 【题型】选择题 【适用】较易 【标题】2010年湖南浏阳一中高一上学期期中考试化学试卷 【关键字标签】溶液,离子浓度 【结束】 6【题文】下列离子方程式中书写正确的是( )
【答案】B 【解析】略 【题型】选择题 【适用】较易 【标题】2010年湖南浏阳一中高一上学期期中考试化学试卷 【关键字标签】离子方程式,氢氧化钡 【结束】 7【题文】已知有如下反应:①2Fe3++2I-===2Fe2++I2 ②2Fe2++Br2===2Fe3++2Br- ③2Fe(CN)+I2===2Fe(CN)+2I-,试判断氧化性强弱顺序正确的是
【答案】C 【解析】略 【题型】选择题 【适用】较易 【标题】2010年湖南浏阳一中高一上学期期中考试化学试卷 【关键字标签】氧化性,顺序 【结束】 8【题文】实验室制取少量N2常利用的反应是NaNO2+NH4ClNaCl+N2↑+2H2O,关于该反应的说法正确的是
【答案】A 【解析】略 【题型】选择题 【适用】较易 【标题】2010年湖南浏阳一中高一上学期期中考试化学试卷 【关键字标签】实验室,氧化剂 【结束】 9【题文】用托盘天平称量固体物质时,若将样品和砝码放在托盘上的位置颠倒,平衡时托盘上的砝码质量为10g,游码为0.5g,则样品的质量为
【答案】D 【解析】略 【题型】选择题 【适用】较易 【标题】2010年湖南浏阳一中高一上学期期中考试化学试卷 【关键字标签】托盘天平,砝码 【结束】 10【题文】将26克含有SiO2和CaCO3固体在高温下加热至质量不再改变,冷却后称重为17.2克。(已知:SiO2 + CaCO3 CaSiO3 + CO2↑,SiO2和CaSiO3均为固体) (1)求生成的CO2的体积(标准状况下) (2)求原混合物中所含SiO2的质量。 【答案】(1)4.48L (2)6克 【解析】略 【题型】计算题 【适用】较易 【标题】2010年湖南浏阳一中高一上学期期中考试化学试卷 【关键字标签】高温,体积 【结束】 |
下列各装置中,能构成原电池的是 ( )
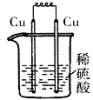



A B C D
【解析】构成原电池的条件是活泼性不同的金属或金属和非金属,导线相连插入电解质溶液中。A和B中电极相同,D中两电极没有插入到同一份溶液中,没有构成完整的闭合回路,所以正确的答案是C。
下图是元素周期表短周期的一部分,下列说法中正确的是( )

A.元素①位于第二周期第ⅣA族
B.气态氢化物的稳定性:④>②
C.最高价氧化物对应水化物的酸性:⑤>④
D.元素的最高正化合价:③=⑤
【解析】考查元素周期表的结构和元素周期律的应用。根据元素在周期表中的位置可判断①~⑤分别是N、O、F、S、Cl。同主族元素自上而下非金属性逐渐减弱,所以水的稳定性要强于H2S的。同周期元素自左向右非金属性逐渐增强,所以选项C是正确的,氟元素没有正价,D不正确。答案选C。
在检验SO42-的过程中,下列操作中正确的是( )
A.先加入稀硝酸,没有产生沉淀,然后再加硝酸钡,产生白色沉淀,证明有SO42-存在
B.先加入硝酸钡,产生白色沉淀,然后再加稀硝酸,沉淀不溶解,证明有SO42-存在
C.先加入稀盐酸,没有产生沉淀,然后再加氯化钡,产生白色沉淀,证明有SO42-存在
D.先加入氯化钡,产生白色沉淀,然后再加稀盐酸,沉淀不溶解,证明有SO42-存在
【解析】在检验SO42-时,必须首先排出其他离子的干扰,所以要先加入盐酸,若没有现象,再加入氯化钡溶液来检验。硝酸具有氧化性,因此若含有SO32-,则被氧化生成SO42-,因此无法证明原溶液中是否SO42-,因此正确的答案是C。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com