氯气是一种重要的工业原料.
Ⅰ.实验室可用二氧化锰和浓盐酸反应制取氯气,反应的化学方程式是
MnO
2+4HCl(浓)
MnCl
2+Cl
2↑+2H
2O
MnO
2+4HCl(浓)
MnCl
2+Cl
2↑+2H
2O
.
Ⅱ.某研究性学习小组查阅资料得知,漂白粉与硫酸反应可制取氯气,化学方程式为:
Ca(ClO)
2+CaCl
2+2H
2SO
42CaSO
4+2Cl
2↑+2H
2O
他们利用该反应设计如下制取氯气并验证其性质的实验.
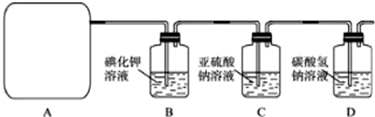
回答下列问题:
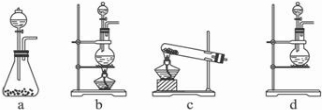
(1)该实验中A部分的装置是
b
b
(填标号).
(2)请你帮助他们设计一个实验,证明洗气瓶C中的Na
2SO
3已被氧化(简述实验步骤):
取少量溶液置于洁净的试管中,向其中滴加稀盐酸至不再产生气体,再向其中滴入氯化钡溶液,若产生白色沉淀,证明亚硫酸钠被氧化
取少量溶液置于洁净的试管中,向其中滴加稀盐酸至不再产生气体,再向其中滴入氯化钡溶液,若产生白色沉淀,证明亚硫酸钠被氧化
.
(3)写出D装置中发生反应的离子方程式
Cl2+H2O═H++Cl-+HClO;H++HCO3-═CO2↑+H2O
Cl2+H2O═H++Cl-+HClO;H++HCO3-═CO2↑+H2O
.
(4)该实验存在明显的缺陷,请你提出改进的方法
应将尾气通入NaOH溶液中
应将尾气通入NaOH溶液中
.
(5)该小组又进行了如下实验:称取漂白粉2.0g,研磨后溶解,配制成250mL溶液,取出25mL加入到锥形瓶中,再加入过量的KI溶液和过量的H
2SO
4溶液,静置.待完全反应后,用0.1mol?L
-1的Na
2S
2O
3溶液作标准液滴定反应生成的碘,已知反应方程式为:2Na
2S
2O
3+I
2═Na
2S
4O
6+2NaI,共用去Na
2S
2O
3溶液20.0mL.则该漂白粉中Ca(ClO)
2的质量分数为
35.75%
35.75%
.



