
题目列表(包括答案和解析)
下列关系图中,A是一种正盐,B是气态氢化物,C是单质,F是强酸。当X无论是强酸还是强碱时都有如下转化关系(其他反应产物及反应所需条件均已略去),当X是强碱时,过量的B跟Cl2反应除生成C外,另一产物是盐酸盐。下列说法中不正确的是:
A.当X是强酸时,A、B、C、D、E、F中均含同一种元素,F可能是H2SO4
B.当X是强碱时,A、B、C、D、E、F中均含同一种元素,F是HNO3
C.B和Cl2的反应是氧化还原反应
D.当X是强酸时,C在常温下是气态单质:
【解析】若F是硫酸,则E是SO3,D是SO2,C是单质硫,则A可以是Na2S,B是硫化氢,A正确。当X是强碱时,A、B、C、D、E、F可以分别是NH4NO3、NH3、N2、NO、NO2、HNO3,B正确。氯气具有强氧化性,而C又是单质,所以反应一定氧化还原反应。所以选项D是错误的,答案选D。
下列关于阿伏加德罗常数NA的说法正确的是( )
A.在铜与硫的反应中,1mol铜失去的电子数为2NA。
B.Cu与足量浓HNO3反应转移NA电子生成的气体在标况下占22.4L(忽略气体溶解及逸散)。
C.31g白磷中含有P—P键的个数为4NA
D.足量Fe与一定量热的浓H2SO4反应放出l mol气体时转移的电子数为2NA(忽略气体溶解及逸散)。
【解析】硫的氧化性比较弱,和铜反应生成的是Cu2S,因此1mol铜失去的电子数为NA。铜和浓硝酸反应的方程式为3Cu+8HNO3=3Cu(NO3)2+4H2O+2NO2↑,即每生成2molNO2转移电子是6mol,因此选项B是错误的。白磷是正四面体结构,1个白磷分子中含有6个P-P键,31g白磷是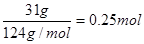 ,所以含有的P—P键为0.25mol×6=1.5mol,D不正确。因为铁是过量的,所以生成物是硫酸亚铁,即铁和浓硫酸反应的方程式为Fe+2H2SO4(浓)
,所以含有的P—P键为0.25mol×6=1.5mol,D不正确。因为铁是过量的,所以生成物是硫酸亚铁,即铁和浓硫酸反应的方程式为Fe+2H2SO4(浓)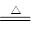 FeSO4+H2O+SO2↑,所以选项D是正确的。答案选D。
FeSO4+H2O+SO2↑,所以选项D是正确的。答案选D。
下列关于阿伏加德罗常数NA的说法正确的是( )
A.在铜与硫的反应中,1mol铜失去的电子数为2NA。
B.Cu与足量浓HNO3反应转移NA电子生成的气体在标况下占22.4L(忽略气体溶解及逸散)。
C.31g白磷中含有P—P键的个数为4NA
D.足量Fe与一定量热的浓H2SO4反应放出l mol气体时转移的电子数为2NA(忽略气体溶解及逸散)。
【解析】硫的氧化性比较弱,和铜反应生成的是Cu2S,因此1mol铜失去的电子数为NA。铜和浓硝酸反应的方程式为3Cu+8HNO3=3Cu(NO3)2+4H2O+2NO2↑,即每生成2molNO2转移电子是6mol,因此选项B是错误的。白磷是正四面体结构,1个白磷分子中含有6个P-P键,31g白磷是![]() ,所以含有的P—P键为0.25mol×6=1.5mol,D不正确。因为铁是过量的,所以生成物是硫酸亚铁,即铁和浓硫酸反应的方程式为Fe+2H2SO4(浓)
,所以含有的P—P键为0.25mol×6=1.5mol,D不正确。因为铁是过量的,所以生成物是硫酸亚铁,即铁和浓硫酸反应的方程式为Fe+2H2SO4(浓)FeSO4+H2O+SO2↑,所以选项D是正确的。答案选D。
2011年3月,日本福岛核电站由于地震损毁而造成放射性物质泄漏,在我国多地检测出极微量的![]() I,关于
I,关于![]() I的下列说法中正确的是( )
I的下列说法中正确的是( )
A.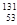 I是放射性核素,应该多吃加碘食盐来预防其对人体的损害
I是放射性核素,应该多吃加碘食盐来预防其对人体的损害
B.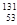 I与
I与![]() I属于碘元素的两种不同核素,互称同素异形体
I属于碘元素的两种不同核素,互称同素异形体
C.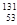 I与
I与![]() I属于同种元素,所以性质完全相同
I属于同种元素,所以性质完全相同
D.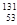 I核内中子数比核外电子数多25个
I核内中子数比核外电子数多25个
【解析】在表示原子的组成时元素符号的左下角表示质子数,左上角表示质量数,因此![]() I的质子数是53,质量数是131,则中子数是131-53=78,所以中子数比核外电子数多78-53=25,选项D是正确的。同素异形体是指同种元素组成的不同单质,B错误。
I的质子数是53,质量数是131,则中子数是131-53=78,所以中子数比核外电子数多78-53=25,选项D是正确的。同素异形体是指同种元素组成的不同单质,B错误。![]() I与
I与![]() I的质量数不同,属于不同的核素,C不正确。食盐加碘是原来预防甲状腺肿大的,A不正确。答案是D。
I的质量数不同,属于不同的核素,C不正确。食盐加碘是原来预防甲状腺肿大的,A不正确。答案是D。
下列各组中顺序的排列不正确的是
A.酸性:HClO4>H2SO4>H3PO4>H2SiO3 B.稳定性:HF>H2O>H2S
C.碱性:KOH >NaOH >Mg(OH)2 D.熔沸点:HI>HBr>HCl>HF
【解析】考查元素周期律的应用。同周期元素自左向右金属性逐渐减弱,非金属性逐渐增强。同主族元素自上而下金属性逐渐增强,非金属性逐渐减弱。金属性越强相应最高价氧化物的水化物的碱性就越强。非金属性越强,相应氢化物的稳定性就越强,最高价氧化物对应水化物的酸性就越强,因此选项ABC均正确。应用HF分子中存在氢键,所以其熔沸点在四种氢化物中是最高的,正确的顺序为HF>HI>HBr>HCl。答案选D。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com