
题目列表(包括答案和解析)
下列推断合理的是( )
A.在常温下,Na2SiO3+H2O+CO2=Na2CO3+H2SiO3↓,说明H2CO3酸性强于H2SiO3;在高温下,Na2CO3+SiO2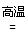 Na2SiO3+CO2↑,说明H2SiO3酸性强于H2CO3
Na2SiO3+CO2↑,说明H2SiO3酸性强于H2CO3
B.c(NH4+)相等的(NH4)2SO4、(NH4)2CO3、(NH4)2Fe(SO4)2溶液,则
c[(NH4)2SO4]>c[(NH4)2CO3] >c[(NH4)2Fe(SO4)2]
C.向1L0.3mol/L的NaOH溶液中缓慢通入CO2气体至溶液增重8.8g时,则溶液中
2c(Na+)=3[c(HCO3-)+c(CO32-)+c(H2CO3)]
D.在海带中提取碘的实验中既可以用四氯化碳作萃取剂也可以用酒精作萃取剂
下列有关海水综合利用的说法正确的是
A. 海水中含有钾元素,只需经过物理变化就可以得到钾单质
B. 海水蒸发制海盐的过程中只发生了化学变化
C. 从海水中可以得到NaCl,电解熔融NaCl可制备Na和Cl2
D. 从海带中提取碘单质的过程不涉及氧化还原反应
下列化学反应方程式或离子方程式书写正确的是
A.乙烯制溴乙烷: CH2CH2 + Br2 → CH2BrCH2Br
B. 乙醇催化氧化:2CH3CH2OH + O2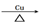 2CH3COH + 2H2O
2CH3COH + 2H2O
C. 苯与氢气加成: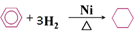
D. 从海带中提取碘:H2O2 + 2I- + 2H+ = I2 + 2H2O
下列推断合理的是( )
A.在常温下,Na2SiO3+H2O+CO2=Na2CO3+H2SiO3↓,说明H2CO3酸性强于H2SiO3;在高温下,Na2CO3+SiO2![]() Na2SiO3+CO2↑,说明H2SiO3酸性强于H2CO3
Na2SiO3+CO2↑,说明H2SiO3酸性强于H2CO3
B.c(NH4+)相等的(NH4)2SO4、(NH4)2CO3、(NH4)2Fe(SO4)2溶液,则
c[(NH4)2SO4]>c[(NH4)2CO3] >c[(NH4)2Fe(SO4)2]
C.向1L0.3mol/L的NaOH溶液中缓慢通入CO2气体至溶液增重8.8g时,则溶液中
2c(Na+)=3[c(HCO3-)+c(CO32-)+c(H2CO3)]
D.在海带中提取碘的实验中既可以用四氯化碳作萃取剂也可以用酒精作萃取剂
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com