
题目列表(包括答案和解析)
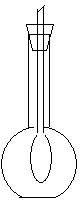
现已用平底烧瓶收集得到CO2,在瓶内有一只扎紧在玻璃管末端的气球,如右图所示。打开塞子迅速往瓶里加入下列物质中的________(填序号),立即塞紧塞子,一段时间后,气球就会自动膨胀起来。
[答案] [提示内容] 此现象表明瓶内的气压变小,气体被消耗。 [详解内容] B.Na2O2 C.KO2 D.RbO3
A.Na2O
Ⅰ栏:实验内容
①确定苯环上是否含有支链 ②确定乙醇中是否含有水 ③确定硬脂酸的酸性 ④确定油脂的不饱和性 ⑤证明淀粉中是否含有葡萄糖
Ⅱ栏:加入的试剂和操作
A.金属Na B.加入CuSO4溶液与KON溶液,生成碱性悬浊液并加热 C.加入无水CuSO4粉末 D.滴加酸性KMnO4溶液 E.滴加Br2水 F.滴加含酚酞的KON溶液并加热
Ⅲ栏:实验现象
a.紫色消失 b.生成蓝色物质 c.产生气体 d.有砖红色沉淀生成 e.蓝色消失 f.红色消失 g.橙色消失
Ⅰ栏 ① ② ③ ④ ⑤
答案 Ⅱ栏
Ⅲ栏
(Ⅰ)目的 (Ⅱ)方案 (Ⅲ)现象
①证明硫酸亚铁溶液已少量氧化变质
②证明硫酸铁中铁离子有较强氧化性
③证明氢氧化亚铁极易被氧化
④证明氯化铁中含有氯离子
A.加入铜片
B.加入硫氰化钾溶液
C.加入铁粉
D.加盐酸
E.加硝酸银溶液和稀硝酸
F.露置于空气中 a.溶液变棕黄色
b.沉淀变红褐色
c.有白色沉淀生成
d.铁粉溶解,溶液变浅绿色
e.溶液变红色
f.铜片溶解,溶液变蓝
答案 (Ⅰ) ① ② ③ ④
(Ⅱ)
(Ⅱ)
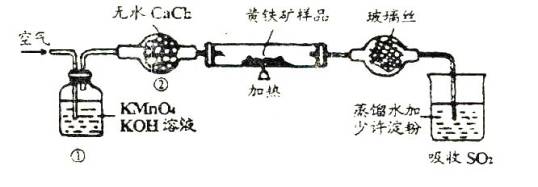
A. 将试管中的样品加热到800—850℃
B. 称取研细的黄铁矿样品
C. 连接全部仪器,使其成为整套试验装置,并检查气密性
D. 将样品小心放入容器中,在将容器小心地推入试管中部
E. 以每分钟1 L的速度鼓入空气
F. 用标准碘液滴定含淀粉的SO2水溶液
(1)正确的试验步骤,其操作编号是 。
(2)装置(1)的作用是 ;装置(2)的作用是 。
(3)碘液跟二氧化硫水溶液发生反应的化学方程式是 。
(4)假定矿样品的硫全部转化为二氧化硫,并全部被水吸收。若称得矿样的质量是0.12克,滴定管中最初读数为0.10mL,末读数为25.60mL,标准碘液的浓度为0.05摩/升,则黄铁矿样品种的含硫量是(列式及答案) 。
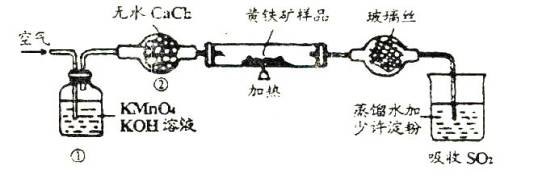
A. 将试管中的样品加热到800—850℃
B. 称取研细的黄铁矿样品
C. 连接全部仪器,使其成为整套试验装置,并检查气密性
D. 将样品小心放入容器中,在将容器小心地推入试管中部
E. 以每分钟1 L的速度鼓入空气
F. 用标准碘液滴定含淀粉的SO2水溶液
(1)正确的试验步骤,其操作编号是 。
(2)装置(1)的作用是 ;装置(2)的作用是 。
(3)碘液跟二氧化硫水溶液发生反应的化学方程式是 。
(4)假定矿样品的硫全部转化为二氧化硫,并全部被水吸收。若称得矿样的质量是0.12克,滴定管中最初读数为0.10mL,末读数为25.60mL,标准碘液的浓度为0.05摩/升,则黄铁矿样品种的含硫量是(列式及答案) 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com