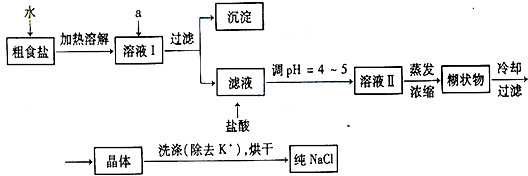
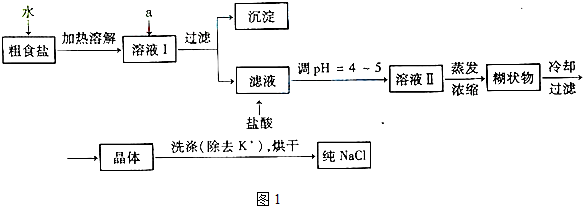
(2011?烟台模拟)食盐是日常生活的必需品,也是重要的化工原料.
(1)粗食盐常含有少量K
+、Ca
2+、Mg
2+、Fe
3+、SO
42-等杂质离子,实验室提纯NaCl的流程如下:

提供的试剂:饱和Na
2CO
3溶液 饱和K
2CO
3溶液 NaOH溶液 BaCl
2溶液 Ba(NO
3)
2溶液
①欲除去溶液Ⅰ中的Ca
2+、Mg
2+、Fe
3+、SO
42-离子,选出A所代表的试剂,按滴加顺序依次为
BaCl2、NaOH、Na2CO3
BaCl2、NaOH、Na2CO3
(只填化学式).
②加盐酸的目的是(用离子方程式表示)
H++OH-═H2O,CO32-+2H+═H2O+CO2↑
H++OH-═H2O,CO32-+2H+═H2O+CO2↑
.
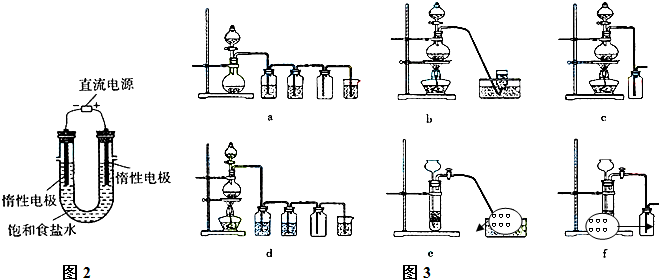
(2)某化学小组拟采用如下装置(夹持和加热仪器已略去)电解饱和食盐水,并用电解产生的H
2还原CuO粉末来测定Cu的相对原子质量,同时验证氯气的氧化性.

①写出甲中反应的化学方程式
.
②为完成上述实验,正确的连接顺序为A连
E
E
,B连
C
C
(填接口字母).
③乙装置中X试剂可以是
淀粉KI溶液
淀粉KI溶液
,丙装置中Y试剂的作用是
吸收氢气中的水
吸收氢气中的水
.
④测定Cu的相对原子质量.
将ω g CuO置于硬质玻璃管中,按以下两个方案测得的数据计算Cu的相对原子质量.
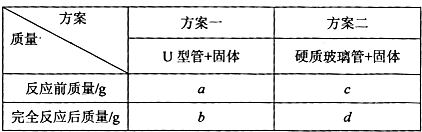
请回答:
你认为方案
二
二
较佳,另一个方案得到的Cu的相对原子质量会
偏低
偏低
填“偏低”、“偏高”).按较佳方案计算,得到Cu的相对原子质量是
.