ЈЁ2008?ҪТСфТ»ДЈЈ©ЈЁ1Ј©ПВГжЛщБРөДКЗЦРС§»ҜС§КөСйКТЦРјёЦЦіЈјыөДТЗЖчЈәИЭБҝЖҝЎўЛбКҪөО¶Ё№ЬЎўјоКҪөО¶Ё№ЬЎўОВ¶ИјЖЎўБҝНІЎўНРЕММмЖҪЎўЖХНЁВ©¶·ЎўІЈБ§°фЎўЙХұӯЈ®
ўЩИфТӘҪшРРЦРәНөО¶ЁКөСйЈ¬»№ИұЙЩөДІЈБ§ТЗЖчКЗ
Ч¶РОЖҝ
Ч¶РОЖҝ
Ј®
ўЪИфТӘУГМјЛбДЖ№ММеЕдЦЖТ»¶ЁОпЦКөДБҝЕЁ¶ИөДМјЛбДЖИЬТәЈ¬»№ИұЙЩөДІЈБ§ТЗЖчКЗ
ҪәН·өО№Ь
ҪәН·өО№Ь
Ј®
ЈЁ2Ј©ДіС§ЙъНщТ»Ц§КФ№ЬЦР°ҙТ»¶ЁөДЛіРт·ЦұрјУИлПВБРјёЦЦИЬТәЈЁТ»ЦЦИЬТәЦ»јУТ»ҙОЈ©Јә
AЈ®KIИЬТә BЈ®өн·ЫИЬТә CЈ®NaOHИЬТә DЈ®ПЎH
2SO
4 EЈ®ВИЛ®Ј®
·ўПЦИЬТәСХЙ«°ҙИзПВЛіРтұд»ҜЈәОЮЙ«ЎъЧШ»ЖЙ«ЎъА¶Й«ЎъОЮЙ«ЎъА¶Й«Ј®
ТАҫЭИЬТәСХЙ«өДұд»ҜЈ¬ЕР¶ПјУИлТФЙПТ©Ж·өДЛіРтКЗЈЁМоРҙРтәЕЈ©
AЎъEЎъBЎъCЎъD
AЎъEЎъBЎъCЎъD
Ј®
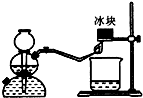
ЈЁ3Ј©ЦЪЛщЦЬЦӘЈ¬ЗвЖшИјЙХЙъіЙЛ®Ј®И»¶шЈ¬ЧКБПұнГчЈ¬ЗвЖшИјЙХКұіэЙъіЙЛ®НвЈ¬»№ЙъіЙБнТ»ІъОпЈ®ДіН¬С§УГИзНјЛщКҫөДКөСйЧ°ЦГЈ¬СйЦӨёГІъОпөДҙжФЪЈ®КөСйІҪЦиј°ПЦПуИзПВЈәЦЖH
2ЎўСйҙҝЈ¬Ҫ«»рСж¶ФЧЕұщҝйЈ®
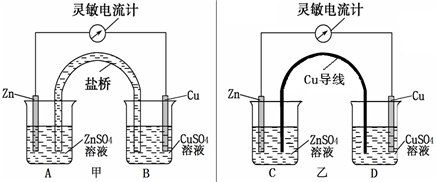
ўЩФЪРЎЙХұӯДЪјУИлУГБтЛбЛб»ҜөДПЎKIөн·ЫИЬТәЈ¬Ҫ«РЎЙХұӯ·ЕФЪұщҝйПВ·ҪЈ¬
№ЫІмөҪЙХұӯЦРИЬТәУЙОЮЙ«ұдіЙБЛА¶Й«Ј®
ўЪФЪБнТ»ёцРЎЙХұӯДЪјУИлУГБтЛбЛб»ҜөДПЎKMn0
4ИЬТәЈ¬Ҫ«РЎЙХұӯ·ЕФЪұщҝйПВ·ҪЈ¬№ЫІмөҪЙХұӯЦРИЬТәұдіЙБЛОЮЙ«Ј®ЗлДгРҙіцБнТ»ІъОпөДҪб№№КҪЈә
H-O-O-H
H-O-O-H
Ј»
УЙЙПКцКөСйЦРҝЙТФ№йДЙіцёГІъОпөД»ҜС§РФЦКУР
Сх»ҜРФәН»№ФӯРФ
Сх»ҜРФәН»№ФӯРФ
Ј®

 H2OЈЁgЈ©+COЈЁgЈ©өДЖҪәвіЈКэK=
H2OЈЁgЈ©+COЈЁgЈ©өДЖҪәвіЈКэK= ўЩФЪРЎЙХұӯДЪјУИлУГБтЛбЛб»ҜөДПЎKIөн·ЫИЬТәЈ¬Ҫ«РЎЙХұӯ·ЕФЪұщҝйПВ·ҪЈ¬
ўЩФЪРЎЙХұӯДЪјУИлУГБтЛбЛб»ҜөДПЎKIөн·ЫИЬТәЈ¬Ҫ«РЎЙХұӯ·ЕФЪұщҝйПВ·ҪЈ¬