
题目列表(包括答案和解析)


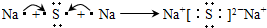
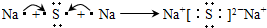

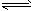 2EB2(g)+O2(g)
2EB2(g)+O2(g) 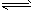 2EB3(g);△H=-197kJ/mol 若将隔板固定在中央,且x=1,达平衡时右室的压强是起始时的0.7倍,则左室反应的平衡常数K=_______________。
2EB3(g);△H=-197kJ/mol 若将隔板固定在中央,且x=1,达平衡时右室的压强是起始时的0.7倍,则左室反应的平衡常数K=_______________。 A、B、C、D、E、F属于短周期主族元素。其中A元素原子是短周期中原子半径最大的原子,B是最小的原子;C元素原子的最外层电子数为m,次外层电子数为n;D元素原子的L层电子数为m+n,M层电子数为m-n;E元素原子的最外层电子数等于其电子层数,且在周期表中与D元素相邻;F元素原子的核外电子数是C元素原子的2倍。A、B、C三种元素可组成化合物X,C、D可组成化合物Y,C、E可组成化合物Z。
(1)写出下列元素的元素符号:B ,
D ,F ;
(2)A~F所形成的简单离子中,与Mg2+具有相同电子层结构的是 。(用离子符号表示);
(3)化合物Z与X的水溶液反应的离子方程式为 ;
(4)化合物Y用途广泛,试列举其中一种用途 。
(8分)A、B、C、D、E、F属于短周期主族元素。其中A元素原子是短周期中原子半径最大的原子,B是最小的原子;C元素原子的最外层电子数为m,次外层电子数为n;D元素原子的L层电子数为m+n,M层电子数为m-n;E元素原子的最外层电子数等于其电子层数,且在周期表中与D元素相邻;F元素原子的核外电子数是C元素原子的2倍。A、B、C三种元素可组成化合物X,C、D可组成化合物Y,C、E可组成化合物Z。
(1)写出下列元素的元素符号:B ,D ,F ;
(2)A~F所形成的简单离子中,与Mg2+具有相同电子层结构的是 。(用离子符号表示);
(3)化合物Z与X的水溶液反应的离子方程式为 ;
(4)化合物Y用途广泛,试列举其中一种用途 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com