
题目列表(包括答案和解析)
(创新)同学们,你们爱吃巧克力吗?你们是否知道,在巧克力中含有一种常见的化学物质——草酸(化学式为C2H2O4).草酸通常以晶体(C2H2O4·2H2O)的形式存在,常温下为固体.以下是某化学兴趣小组提取了草酸晶体之后对其进行研究的过程.
[提出问题]草酸晶体受热分解产生了什么?
[猜想与假设]根据质量守恒定律,草酸晶体分解的产物中可能含水、CO或CO2.
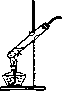
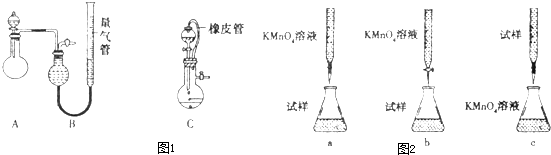
[实验论证]研究小组设计了以下实验装置(如图)对上述猜想进行了探究.

信息提示:装置B为干燥管,其中的无水硫酸铜与水反应会变成蓝色.
(1)装置A中饱和澄清石灰水的作用是________;
(2)若分解产物中存在CO,则装置C中的实验现象是________,该反应的化学方程式为________;
(3)装置E的作用是________.
[反思与评价]
(1)该实验装置在设计上存在一个明显的错误,请你将其指出:________,可以改进的方法是________;
(2)用于草酸晶体分解的实验发生装置如图所示,由此可以推断草酸晶体的一条物理性质是________.

| b |
| a |
| b |
| a |
| 第一次滴定 | 第二次滴定 | 第三次滴定 | |
| 消耗标准盐酸的体积(mL) | 24.98 | 25.00 | 25.02 |
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com