
题目列表(包括答案和解析)
| 阳离子 | K+ Ba2+ Ag+ Mg2+ NH
| ||||||||
| 阴离子 | SO
|
| 排除的离子 | 排除的依据 | ||
NH
|
由于溶液呈碱性,且未嗅到刺激性气味,碱性溶液中无沉淀生成 |
| 肯定存在的离子 | |
| 简述判断依据 | |
| 排除的离子 | |
| 简述排除的依据 |
| 尚待检验的离子 | |
| 简述检验方法 |
| 阳离子 | K+ Ba2+ Ag+ Mg2+ NH4+ Na+ |
| 阴离子 | SO42- SO32- CO32- AlO2- |
| 阳离子 | Ag+ Na+ Fe3+ Al3+ Ba2+ | ||||
| 阴离子 | OH- Cl- S
|
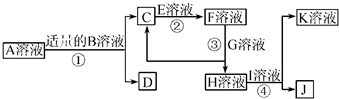 物质A~K都是由下表中的离子形成的,且为中学化学常见物质,有如图所示的转化关系.部分产物中的水已省略.(如果需要、阴、阳离子可以重复使用)
物质A~K都是由下表中的离子形成的,且为中学化学常见物质,有如图所示的转化关系.部分产物中的水已省略.(如果需要、阴、阳离子可以重复使用)| 阳离子 | Na+ Al3+ Ag+ Ba2+ | 阴离子 | OH- Cl- SO42- AlO2- NO3- |
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com