浅绿色的硫酸亚铁铵晶体[又名莫尔盐(NH
4)
2SO
4?FeSO
4?6H
2O]比绿矾(FeSO
4?7H
2O)更稳定,常用于定量分析.莫尔盐的一种实验室制法如下:
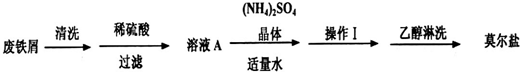
(1)向废铁屑中加入稀硫酸后,并不等铁屑完全溶解而是剩余少量时就进行过滤,其目的是
防止Fe2+离子被氧化为Fe3+离子
防止Fe2+离子被氧化为Fe3+离子
;
证明溶液A不含Fe
3+离子的最佳试剂是
b
b
(填序号字母).
a.酚酞溶液 b.KSCN溶液 c.烧碱溶液 d.KMnO
4溶液
操作I的步骤是:加热蒸发、
冷却结晶
冷却结晶
、过滤.
(2)浓度均为0.1mol?L
-1莫尔盐溶液和(NH
4)
2SO
4溶液,c(NH
4+)前者大于后者,原因是
莫尔盐中的Fe2+离子易水解,趋使溶液显酸性,抑制NH4+水解,故c(NH4+)前者大于后者
莫尔盐中的Fe2+离子易水解,趋使溶液显酸性,抑制NH4+水解,故c(NH4+)前者大于后者
.
(3)用托盘天平称量(NH
4)
2SO
4晶体,晶体要放在天平
左
左
(填“左”“右”)盘.
(4)从下列装置中选取必要的装置制取(NH
4)
2SO
4溶液,连接的顺序(用接口序号字母表示)是:a接
d
d
;
e
e
接
f
f
.
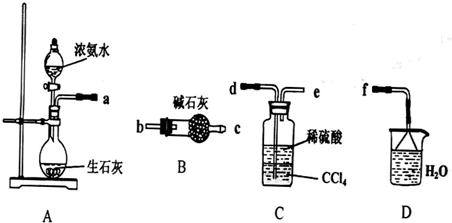
将装置C中两种液体分离开的操作名称是
分液
分液
.装置D的作用是
吸收多余的NH3防止污染空气,防止倒吸
吸收多余的NH3防止污染空气,防止倒吸
.

 在一烧杯中盛有稀硫酸,有一塑料小球(与酸、碱均不发生反应)悬浮于溶液中,如图所示.
在一烧杯中盛有稀硫酸,有一塑料小球(与酸、碱均不发生反应)悬浮于溶液中,如图所示.
