
题目列表(包括答案和解析)
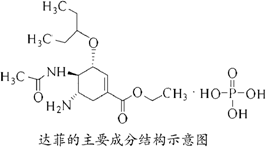 (12分)目前大爆发的H5N1亚型高致病性禽流感令全球震惊,它不仅威胁鸟类生存也危及人类生命。其中H是血凝素(Hemagglutinin),而N是神经氨酸酶(Neyramidinase),这两种物质在病毒入侵细胞传播的过程中起着极为重要的作用。H是病毒入侵的“开路先锋”,它能和细胞上的蛋白质结合,在细胞膜上打开一个通道,使该病毒能进入细胞进行自我复制,制造出一类新病毒。而进入细胞的功臣H却要与宿主细胞膜“纠缠不清”,此时,N通过“水解”方式切断病毒和宿主细胞,再次去寻找下一个感染目标。现在著名的“达菲”(达菲的主要成分是C16H28N2O4H3PO4,结构如下图所示)作用原理就是使新的病毒无法脱离宿主细胞,从而抑制病毒。今天各国政府及其科学家正在积极研制抗H5N1病毒的疫苗。研究发现,在注射其低剂量疫苗的同时要注射促进免疫性产生的化学辅剂化合物(ABC2?12H2O)方能产生免疫性,以达到预防为主的目的。
(12分)目前大爆发的H5N1亚型高致病性禽流感令全球震惊,它不仅威胁鸟类生存也危及人类生命。其中H是血凝素(Hemagglutinin),而N是神经氨酸酶(Neyramidinase),这两种物质在病毒入侵细胞传播的过程中起着极为重要的作用。H是病毒入侵的“开路先锋”,它能和细胞上的蛋白质结合,在细胞膜上打开一个通道,使该病毒能进入细胞进行自我复制,制造出一类新病毒。而进入细胞的功臣H却要与宿主细胞膜“纠缠不清”,此时,N通过“水解”方式切断病毒和宿主细胞,再次去寻找下一个感染目标。现在著名的“达菲”(达菲的主要成分是C16H28N2O4H3PO4,结构如下图所示)作用原理就是使新的病毒无法脱离宿主细胞,从而抑制病毒。今天各国政府及其科学家正在积极研制抗H5N1病毒的疫苗。研究发现,在注射其低剂量疫苗的同时要注射促进免疫性产生的化学辅剂化合物(ABC2?12H2O)方能产生免疫性,以达到预防为主的目的。
该化学辅剂ABC2?12H2O中,A是正一价金属离子,B是正三价金属离子,C为负二价阴离子基团。A单质与过量氧气反应的生成物D常用于急救器和消防员背包中,以消除呼出的CO2和湿气并提供O2。A还是动植物生长所必需的元素,同植物光合作用和呼吸作用有关。c.o. B加入茜素[C14H6O2 (OH)2]的氨溶液中,先生成白色沉淀,后能生成红色沉淀[B(C14H7O4)3],从而鉴定之。B溶液中加入NaOH先生成白色沉淀,继续加入NaOH时,沉淀又溶解。C与Ba2+在酸性溶液中生成白色沉淀而可相互鉴定之。
(1)该化学辅剂的化学式为 ,俗名是 ;
(2)达菲的主要成分中含有的官能团为 (填序号);
a.苯基 b. 酯基 c. 氨基 d. 酰氨基 e.羧基 f. 烷烃基 g.磷酸根
(3)写出D用于急救器和消防员背包中的有关反应的化学方程式:
;
(4)写出B与茜素的氨溶液反应的化学方程式:
;
(5)根据该题所给出的信息,请指出化学工作者可以设计及合成具有哪三类效能的化合物用以防治禽流感?
。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com