
题目列表(包括答案和解析)

| Cu |
| △ |
| Cu |
| △ |



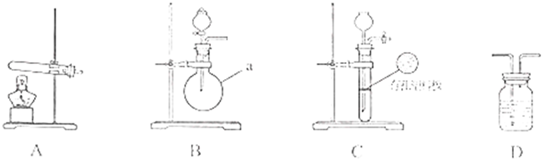
| 实验装置 | 实验药品 | 制备原理 | |||||||||
| 甲小组 | A | 氢氧化钙、硫酸铵 | 反应的化学方程式为 ① (NH4)2SO4+Ca(OH)2
(NH4)2SO4+Ca(OH)2
| ||||||||
| 乙小组 | ② B B |
浓氨水、氢氧化钠 | 用化学平衡原理分析氢氧化钠的作用: ③ 氢氧化钠溶于氨水后放热、增加氢氧根浓度,使NH3+H2O?NH3?H2O?NH4++OH-向逆方向移动,加快氨气逸出 氢氧化钠溶于氨水后放热、增加氢氧根浓度,使NH3+H2O?NH3?H2O?NH4++OH-向逆方向移动,加快氨气逸出 |
有一种白色粉末由等质量的两种物质混合而成,分别取适量该白色粉末置于三支试管中进行实验。
(1)逐滴加入6 mol·L-1盐酸,同时不断振荡试管,有气泡产生,反应结束后得到无色透明溶液;
(2)加热试管中的白色粉末,试管口有水滴凝结;
(3)逐滴加入6 mol·L-1硫酸,同时不断振荡试管,有气泡产生,反应结束后试管中还有白色不溶物。
下列混合物符合以上实验现象的是( )
A.NaHCO3、AgNO3 B.BaCl2、MgCO3
C.NH4HCO3、MgCl2 D.CaCl2·6H2O、Na2CO3
(1)逐滴加入6 mol·L-1盐酸,同时不断振荡试管,有气泡产生,反应结束后得到无色透明溶液
(2)加热试管中的白色粉末,试管口有水滴凝结
(3)逐滴加入6 mol·L-1硫酸,同时不断振荡试管,有气泡产生,反应结束后试管中还有白色不溶物
则这种白色粉末是( )
A.CaCl2·6H2O、Na2CO3 B.NaHCO3、AgNO3
C.NH4HCO3、MgCl2 D.BaCl2、MgCO3
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com