(2013?金华模拟)某物质M具有热导率高、高温下电绝缘性好、高温下材料强度大、无毒等优异性能.经检测,M中只含有两种短周期元素.现取82gM溶于适量的NaOH溶液中恰好反应,得到无色溶液A和44.8L气体B(气体体积为标准状况下),该气体能使红色石蕊试纸变蓝.往反应后的溶液中逐滴加入盐酸,可观察到溶液先变浑浊后变澄清.
物质B有如下转化关系:B
C
D
EE是一种强酸.将c和D的混合物溶解在接近零度的水中,即可得到一种弱酸F的水溶液.请回答下列问题:
(1)物质M的化学式为
AlN
AlN
,属于
原子
原子
晶体(填“分子”、“离子”、“原子”等).
(2)无色溶液A呈碱性,其原因是
AlO2-+2H2O=Al(OH)3+OH-
AlO2-+2H2O=Al(OH)3+OH-
(用离子方程式表示).
(3)弱酸F是一种比醋酸酸性稍强的弱酸,很不稳定,通常在室温下易分解.要制得F溶液,可以往冷冻的其钠盐浓溶液中加入或通入某种物质,下列物质不适合使用的是
bd
bd
(填序号).
a.盐酸 b.二氧化碳 c.稀硫酸 d.二氧化硫
(4)工业碱性废水中若含有NO
-2,可用铝粉除去.已知此反应体系中检测到B气体.写出上述反应的离子方程式
2Al+NO2-+OH-+H2O=2AlO2-+NH3↑
2Al+NO2-+OH-+H2O=2AlO2-+NH3↑
.若改用电解法将废水中NO
-2转换为N
2除去,N
2将在
阴极
阴极
(填“阴极”或“阳极”)生成,电极反应为
2NO2-+6e-+4H2O=N2+8OH-
2NO2-+6e-+4H2O=N2+8OH-
.
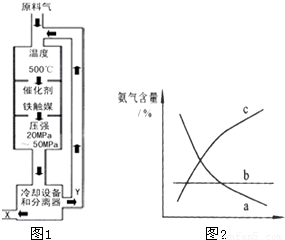
(5)现发现一种活性很强的化合物G,其组成为NH
5,G遇水能产生两种气体,其中一种气体为B,则物质G的电子式为
.



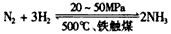 △H <0,生产流程如图所示。
△H <0,生产流程如图所示。 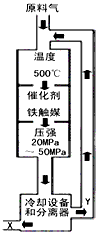
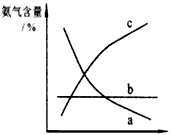
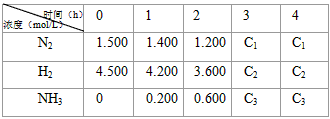
 N2(g)+3H2(g)的平衡常数______________。
N2(g)+3H2(g)的平衡常数______________。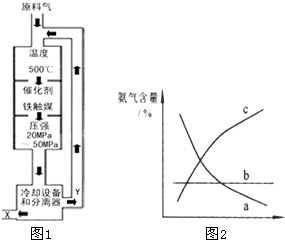 (1)合成氨工业对化学工业和国防工业具有重要意义.工业合成
(1)合成氨工业对化学工业和国防工业具有重要意义.工业合成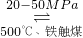 2NH3△H<0,生产流程如图1所示.
2NH3△H<0,生产流程如图1所示. 2NH3△H<0,生产流程如图1所示.
2NH3△H<0,生产流程如图1所示.