
题目列表(包括答案和解析)
已知A、B、D、E均为中学化学常见单质及化合物,它们之间的转化关系如图所示(部分产物略去)
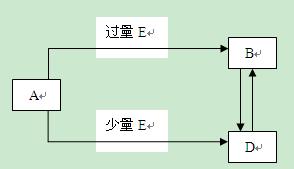
(1)若A和E均为单质且B物质为极性键形成的非极性分子。B的结构式为____。
(2)若A为可溶性强碱(MOH),E为同主族元素形成的常见非金属化合物,且该化合物中两种元素的质量比为1:1,试写出A到B的化学方程式______。
(3)若取B的溶液装于试管,向溶液中滴加KSCN溶液,无明显现象,再滴加稀盐酸,产生红色溶液,则用化学方程式表示工业制备E化学原理______;D的溶液中含有少量B,用离子方程式表示除杂方法_______。
(4)若A由同一短周期的两种元素组成,D为白色沉淀,且A、B溶液混合生成D,试写出A到B的化学方程式______;A、B溶液混合生成D的离子方程式为______。
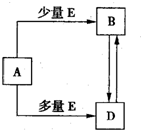 已知A、B、D、E均为中学化学常见单质或化合物,它们之间的关系如图所示(部分产物略去).
已知A、B、D、E均为中学化学常见单质或化合物,它们之间的关系如图所示(部分产物略去).
| ||
| ||
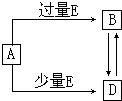 已知A、B、D、E均为中学化学常见单质或化合物,它们之间的关系如图所示(部分产物略去).
已知A、B、D、E均为中学化学常见单质或化合物,它们之间的关系如图所示(部分产物略去).已知A、B、D、E均为中学化学常见单质或化合物,它们之间的关系如图所示(部分产物略去)。
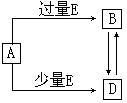
(1)若A和E为单质,组成A单质的元素是自然界中形成化合物种类最多的元素。
①写出B分子的结构式 ,B分子中各原子最外层是否都满足8电子结构? (填“是”或“否”)。
②向50mL4mol/L的NaOH溶液中通入1.12L气体B(标准状况),反应后溶液中溶质的物质的量之比为 (填化学式及其物质的量之比)。
③4gA完全燃烧放出131.2kJ的热量,写出表示A的燃烧热的热化学方程式 。
(2)若A为第三周期某元素的氯化物,0.1mol/LE的水溶液pH=13,且其焰色反应颜色呈黄色。
①E的化学式 ,E中含有的化学键类型为 。
②写出图中A的溶液→B的溶液的离子方程式 。
已知A、B、D、E均为中学化学常见单质或化合物,它们之间的关系如图所示(部分产物略去)。
(1)若A和E为单质,组成A单质的元素是自然界中形成化合物种类最多的元素。
①写出B分子的结构式 ,B分子中各原子最外层是否都满足8电子结构? (填“是”或“否”)。
②向50mL4mol/L的NaOH溶液中通入1.12L气体B(标准状况),反应后溶液中溶质的物质的量之比为 (填化学式及其物质的量之比)。
③4gA完全燃烧放出131.2kJ的热量,写出表示A的燃烧热的热化学方程式 。
(2)若A为第三周期某元素的氯化物,0.1mol/LE的水溶液pH=13,且其焰色反应颜色呈黄色。
①E的化学式 ,E中含有的化学键类型为 。
②写出图中A的溶液→B的溶液的离子方程式 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com