
题目列表(包括答案和解析)
(福建师大附中2008-2009学年高三第一学期第一学段检测,化学,22)(1)用5.0mol/L的NaOH溶液配制2.0mol/L的NaOH溶液时,下图所示的仪器中,肯定不需要的是 (填序号),配制上述溶液还需要的玻璃仪器是 (填仪器名称)。
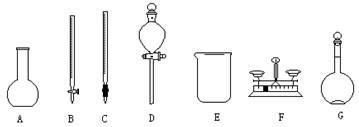
(2)在配制过程中,下列操作将导致实际所配NaOH溶液浓度偏低的是(填编号) _ _。
①准确取出的浓NaOH溶液在空气中露置时间过长;②用量器将浓NaOH溶液直接加入容量瓶,缓慢加入蒸馏水至液面最低点恰好和环形刻度线相切;③摇匀后,液面低于刻度线,再加蒸馏水至液面最低点恰好和环形刻度线相切;④用于稀释NaOH溶液的仪器未洗涤。
(安徽师大附中2008年第一次模拟考试,化学,14)下列除去杂质的方法中,正确的是
A.除去铜粉中混有的铁:加足量稀硝酸,过滤
B.除去N2中少量的CO:通过足量灼热的CuO粉末
C.除去KCl溶液中的少量CaCl2:加适量Na2CO3溶液,过滤
D.除去CO2中的少量的HCl:通过足量的饱和碳酸氢钠溶液
(08福建师大附中模拟)能正确表示下列反应的离子方程式是 ( )
A.过量铁与稀硝酸反应:Fe+4H++NO3-=Fe3++2H2O+NO↑
B.碳酸氢钠溶液与少量石灰水反应:HCO3-+Ca2++OH-=CaCO3↓+H2O
C.在AlCl3溶液中加入过量氨水:Al3++3NH3?H2O=Al(OH)3↓+3NH4+
D.在硫酸氢钾溶液中加入氢氧化钡溶液至pH=7:Ba2++OH-+H++SO42-=BaSO4↓+H2O
(08福建师大附中模拟)实验室中,用如下图所示装置及所给药品(图中部分夹持仪器已略去)探究工业制硫酸接触室中的反应,并测定此条件下二氧化硫的转化率。已知SO3熔点为16.8℃,假设气体进入装置时分别被完全吸收,且忽略装置内空气中的CO2。
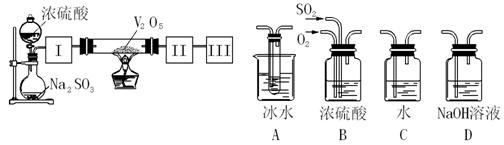
(1)已知0.5molSO2被O2氧化成气态SO3,放出49.15 kJ热量,反应的热化学方程式为__________ 。
(2)根据实验目的,请从上面右图中选择Ⅰ、Ⅱ、Ⅲ处合适的装置,将其序号填入空格中:装置Ⅰ ,装置Ⅱ ,装置Ⅲ 。
(3)开始进行实验时,首先应进行的操作是 。
(4)加热硬质玻璃管时,若不断升高温度,SO2的转化率会 (填“增大”、“不变”或“减小”)。
(5)停止通入SO2,熄灭酒精灯后,为使残留在装置中的SO2、SO3被充分吸收,操作方法为______。
(6)实验结束后,若装置Ⅱ增加的质量为b g ,装置Ⅲ增加的质量为a g,则此条件下二氧化硫的转化率是 (用含字母的代数表示)。
(08福建师大附中模拟)有一未完成的离子方程式: ![]() +XO3-+6H+=3X2+3H2O,据此判断:X元素的最高化合价为( )
+XO3-+6H+=3X2+3H2O,据此判断:X元素的最高化合价为( )
A.+7 B.+5 C.+4 D.+1
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com