
题目列表(包括答案和解析)

(1)粗盐中含有Ca2+、Mg2+、![]() 等杂质离子,精制时所用试剂为:A.盐酸;B.BaCl2溶液;C.NaOH溶液;D.Na2CO3溶液。则加入试剂的顺序是_________________。(填序号)
等杂质离子,精制时所用试剂为:A.盐酸;B.BaCl2溶液;C.NaOH溶液;D.Na2CO3溶液。则加入试剂的顺序是_________________。(填序号)
(2)写出用海滩上的贝壳制Ca(OH)2的化学方程式:__________________,_________________。
(3)电解无水MgCl2可制取镁和Cl2,其中副产品Cl2和粉末状熟石灰可制得漂白粉。制漂白粉的化学方程式为______________________________________________________________。
(4)用海滩上的贝壳制Ca(OH)2,而不从异地山中开凿石灰石制取,主要考虑到什么问题?_______________________________________。
(5)从经济效益角度看,该化工厂厂址应选在___________________________。

试回答下列问题:
(1)粗盐中含有Ca2+、Mg2+、![]() 等杂质离子,精制时所用试剂为:A.盐酸 B.BaCl2溶液 C.NaOH溶液 D.Na2CO3溶液。则加入试剂的顺序是____________________________。
等杂质离子,精制时所用试剂为:A.盐酸 B.BaCl2溶液 C.NaOH溶液 D.Na2CO3溶液。则加入试剂的顺序是____________________________。
(2)写出电解饱和食盐水的化学反应方程式。
(3)写出用海滩上贝壳制Ca(OH)2的化学反应方程式。
(4)由MgCl2·6H2O脱水制无水MgCl2用于电解,MgCl2·6H2O晶体在________气体中加热脱水,生产中通入此种气体的作用是______________________________________________。
(5)电解无水MgCl2可制取金属镁和氯气,其中副产品氯气和粉末状熟石灰反应可制得漂白粉。制漂白粉的化学反应方程式为_______________________________________________。
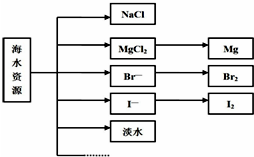 海水中可提取多种化工原料,下面是工业上对海水的几项综合利用示意图.
海水中可提取多种化工原料,下面是工业上对海水的几项综合利用示意图.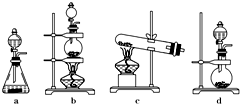
海水中可提取多种化工原料,下面是工业上对海水的几项综合利用示意图。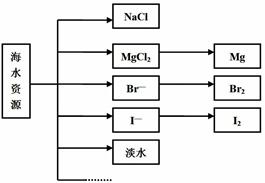
按要求回答问题:
(1)浩瀚的海洋是一个巨大的宝库,蕴含有80多种元素,可供提取利用的有50多种。下列物质不需要通过化学变化就能够从海水中获得的是 。
A.食盐 B.金属钠 C.淡水
(2)以电解食盐水为基础制取Cl2、 等产品的工业称为“氯碱工业”。
(3)实验室制取氯气的反应原理为:MnO2+4HCl(浓) MnCl2+Cl2↑+2H2O;根据上述实验原理,从下列装置中选择合适的发生装置用于实验室制取少量氯气
MnCl2+Cl2↑+2H2O;根据上述实验原理,从下列装置中选择合适的发生装置用于实验室制取少量氯气
(填写装置的序号)。
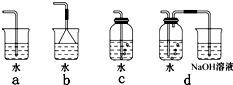
(4)实验室中模拟Br—→Br2的转化,可以通过在KBr溶液中滴加少量新制氯水的实验进行实现。写出Br—→Br2的转化离子方程式为: ;氯水不稳定,要现用现配,下列吸收氯气制备氯水的装置最合理的是 (选填下列选项的编号字母)。
(5)电解熔融氯化镁所得的镁蒸气冷却后即为固体镁。下列气体中,镁蒸气可以在其氛围中冷却的是 (选填下列选项的编号字母)。
A.Cl2 B.N2 C.Ar D.空气 E.H2
海水中可提取多种化工原料,下面是工业上对海水的几项综合利用示意图。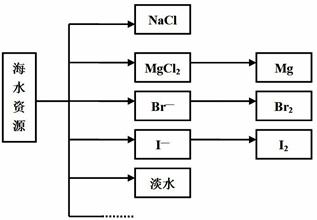
按要求回答问题:
(1)浩瀚的海洋是一个巨大的宝库,蕴含有80多种元素,可供提取利用的有50多种。下列物质不需要通过化学变化就能够从海水中获得的是 。
A.食盐 B.金属钠 C.淡水
(2)以电解食盐水为基础制取Cl2、 等产品的工业称为“氯碱工业”。
(3)实验室制取氯气的反应原理为:MnO2+4HCl(浓) MnCl2+Cl2↑+2H2O;根据上述实验原理,从下列装置中选择合适的发生装置用于实验室制取少量氯气 (填写装置的序号)。
MnCl2+Cl2↑+2H2O;根据上述实验原理,从下列装置中选择合适的发生装置用于实验室制取少量氯气 (填写装置的序号)。
(4)实验室中模拟Br—→Br2的转化,可以通过在KBr溶液中滴加少量新制氯水的实验进行实现。写出Br—→Br2的转化离子方程式为: ;氯水不稳定,要现用现配,下列吸收氯气制备氯水的装置最合理的是 (选填下列选项的编号字母)。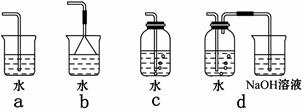
(5)电解熔融氯化镁所得的镁蒸气冷却后即为固体镁。下列气体中,镁蒸气可以在其氛围中冷却的是 (选填下列选项的编号字母)。
A.Cl2 B.N2 C.Ar D.空气 E.H2
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com