
题目列表(包括答案和解析)
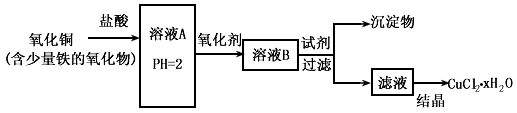
用含少量铁的氧化物的氧化铜制取氯化铜晶体(CuCl2 xH2O)。有如下操作:
xH2O)。有如下操作:
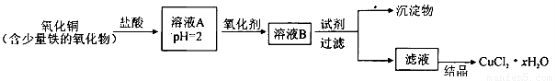
已知:在pH为4~5时,Fe3+几乎完全水解而沉淀,而此时Cu2+却几乎不水解。
(1)溶液A中的金属离子有Fe3+、Fe2+、Cu2+。检验溶液A中Fe2+的最佳试剂为_____(填编号,下同)。
①KMnO4?? ②(NH4)2S??????? ③NaOH???????? ④ KSCN
(2)氧化剂可选用_________。①Cl2? ②KMnO4? ③HNO3? ④H2O2
(3)要得到较纯的产品,试剂可选用_______________。①NaOH ②FeO ③CuO ④Cu2(OH)2CO3
(4)从滤液经过结晶得到氯化铜晶体的方法是_____________(按实验先后顺序选填编号)。
①过滤 ②蒸发浓缩 ③蒸发至干 ④冷却
(5)欲测定溶液A中的Fe2+的浓度,实验前,首先要配制一定物质的量浓度的KMnO4溶液250mL,配制时需要的仪器除天平、玻璃棒、烧杯、药匙、胶头滴管外,还需_________,下列滴定方式中,最合理的是___________(夹持部分略去)(填字母序号)。

(6)为了测定制得的氯化铜晶体(CuCl2 xH2O)中的x值,某学生设计了两种实验方案:
xH2O)中的x值,某学生设计了两种实验方案:
方案一:称取mg晶体灼烧至质量不再减轻为止,冷却、称量所得无水CuCl2的质量为n1g
方案二:称取mg晶体溶于水,加入足量氢氧化钠溶液、过滤、沉淀洗涤后用小火加热至质量不再减轻为止,冷却,称量所得固体的质量为n2g。
试评价上述两种实验方案:其中正确的方案是________,理由是___________,据此计算得x=_________(用含m、n1或n2的代数式表示)。
用含少量铁的氧化物的氧化铜制取氯化铜晶体(CuCl2 xH2O)。有如下操作:
xH2O)。有如下操作: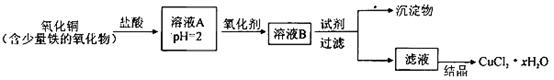
已知:在pH为4~5时,Fe3+几乎完全水解而沉淀,而此时Cu2+却几乎不水解。
(1)溶液A中的金属离子有Fe3+、Fe2+、Cu2+。检验溶液A中Fe2+的最佳试剂为_____(填编号,下同)。
①KMnO4 ②(NH4)2S ③NaOH ④ KSCN
(2)氧化剂可选用_________。①Cl2 ②KMnO4 ③HNO3 ④H2O2
(3)要得到较纯的产品,试剂可选用_______________。①NaOH ②FeO ③CuO ④Cu2(OH)2CO3
(4)从滤液经过结晶得到氯化铜晶体的方法是_____________(按实验先后顺序选填编号)。
①过滤 ②蒸发浓缩 ③蒸发至干 ④冷却
(5)欲测定溶液A中的Fe2+的浓度,实验前,首先要配制一定物质的量浓度的KMnO4溶液250mL,配制时需要的仪器除天平、玻璃棒、烧杯、药匙、胶头滴管外,还需_________,下列滴定方式中,最合理的是___________(夹持部分略去)(填字母序号)。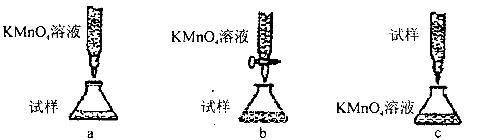
(6)为了测定制得的氯化铜晶体(CuCl2 xH2O)中的x值,某学生设计了两种实验方案:
xH2O)中的x值,某学生设计了两种实验方案:
方案一:称取mg晶体灼烧至质量不再减轻为止,冷却、称量所得无水CuCl2的质量为n1g
方案二:称取mg晶体溶于水,加入足量氢氧化钠溶液、过滤、沉淀洗涤后用小火加热至质量不再减轻为止,冷却,称量所得固体的质量为n2g。
试评价上述两种实验方案:其中正确的方案是________,理由是___________,据此计算得x=_________(用含m、n1或n2的代数式表示)。
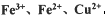 。检验溶液A中含有Fe2+的最佳试剂为_______(填编号,下同)
。检验溶液A中含有Fe2+的最佳试剂为_______(填编号,下同) 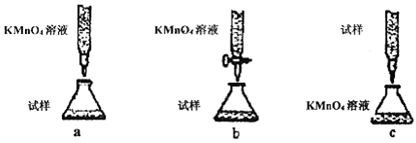
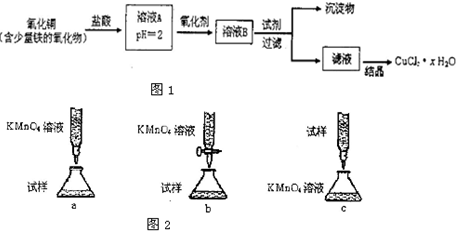
用含少量铁的氧化物的氧化铜制取氯化铜晶体![]() 。有如下操作:
。有如下操作:
已知:在![]() 为4~5时,
为4~5时,![]() 几乎完全水解而沉淀,而此时
几乎完全水解而沉淀,而此时![]() 却几乎不水解。
却几乎不水解。
(1)溶液![]() 中的金属离子有
中的金属离子有![]() 。检验溶液
。检验溶液![]() 中
中![]() 的最佳试剂为 (填
的最佳试剂为 (填
编号,下同)
①![]() ②
②![]() ③
③![]() ④
④![]()
(2)氧化剂可选用
①![]() ②
②![]() ③
③![]() ④
④![]()
(3)要得到较纯的产品,试剂可选用
①![]() ②
②![]() ③
③![]() ④
④![]()
(4)从滤液经过结晶得到氯化铜晶体的方法是 (按实验先后顺序选填编号)
①过滤 ②蒸发浓缩 ③蒸发至干 ④冷却
(5)欲测定溶液![]() 中的
中的![]() 的浓度,实验前,首先要配制一定物质的量浓度的
的浓度,实验前,首先要配制一定物质的量浓度的![]() 溶液
溶液![]() ,配制时需要的仪器除天平、玻璃棒、烧杯、药匙、胶头滴管外,还需 ,
,配制时需要的仪器除天平、玻璃棒、烧杯、药匙、胶头滴管外,还需 ,
下列滴定方式中,最合理的是 (夹持部分略去)(填字母序号)
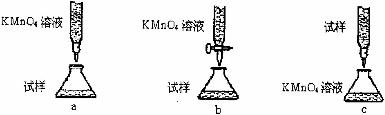 |
(6)为了测定制得的氯化铜晶体![]() 中
中![]() 的值,某兴趣小组设计了两种实验方
的值,某兴趣小组设计了两种实验方
案:
方案一:称取![]() 晶体灼烧至质量不再减轻为止,冷却、称量所得无水
晶体灼烧至质量不再减轻为止,冷却、称量所得无水![]() 的质量为
的质量为![]() g。
g。
方案二:称取![]() 晶体溶于水,加入足量氢氧化钠溶液、过滤、沉淀洗涤后用小火加热至质量不再减轻为止,冷却,称量所得固体的质量为
晶体溶于水,加入足量氢氧化钠溶液、过滤、沉淀洗涤后用小火加热至质量不再减轻为止,冷却,称量所得固体的质量为![]() 。
。
试评价上述两种实验方案:其中正确的方案是 ,据此计算得![]() (用含
(用含![]() 或
或![]() 的代数式表示)。
的代数式表示)。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com