
题目列表(包括答案和解析)
观察金属钠的物理性质及钠与水反应的现象时,你是如何通过观察来认识金属钠的有关物理性质及它跟水的反应的?在观察过程中,你发现了些什么问题?
观察金属钠的物理性质及钠与水反应的现象时,你是如何通过观察来认识金属钠的有关物理性质及它跟水的反应的?在观察过程中,你发现了些什么问题?
研究物质性质的基本方法
1.研究物质性质的基本方法
常有________、________、________、________等.
观察要有明确的________,要对观察到的现象进行________.
2.观察钠的物理性质及钠跟水反应的现象
(1)观察提示
观察盛放在试剂瓶中的金属钠的状态及在煤油中的位置;
切开一块钠,观察钠的切面;亲身感觉钠被切割的难易;
观察钠在水中的位置;
观察钠在水中的状态;
观察钠在水中的运动;
耳听钠与水的反应;
将集满气体的试管移近酒精灯的火焰,耳听声音;
观察溶液颜色的变化.
(2)观察记录
①金属钠的物理性质
②金属钠跟水的反应
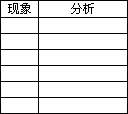
Na与H2O反应的化学方程式为:2Na+2H2O==2NaOH+H2↑.
3.探索Na跟O2的反应

4Na+O2![]() 2Na2O(白色) 2Na+O2
2Na2O(白色) 2Na+O2![]() Na2O2
Na2O2
认识物质物理性质的方法:(1)直接观察;(2)溶解性实验.
(3)借助仪器分析.
在研究金属钠的性质中用到了观察、实验、分类和比较4种方法.
金属的通性:绝大多数金属是银白色固体,有金属光泽,具有延展性,导电、导热性能;绝大多数金属能跟活泼非金属反应,大部分金属能置换出酸中的氢等等.
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com