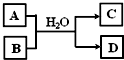
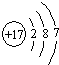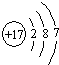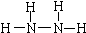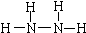X、Y、V、W是常见的短周期元素,它们在周期表里的位置如下图所示.V、W的最简单的气态氢化物M、N混合时有白烟生成,M是碱性气体.请回答以下问题:
(1)W的原子结构示意图为
.
(2)常温常压下,将a L M气体和b L N气体通入水中,若所得溶液的pH=7,则a
>
>
b(填“>、=、<”)
(3)二氧化钛(TiO
2)与X的单质、Y的单质在高温下反应,生成由两种元素组成的两种化合物,该反应的化学方程式为
.
(4)联氨(N
2H
4)也叫肼,是火箭的燃料写出肼的结构式
,用次氯酸钠溶液氧化M能得到肼的稀溶液,写出反应的离子方程式
ClO-+2NH3=N2H4+Cl-+H2O
ClO-+2NH3=N2H4+Cl-+H2O
.
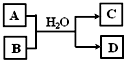
(5)含X元素的一种化合物A与Y的最高价氧化物B之间有右图的转化关系,若D为白色沉淀,则如图转化的离子方程式为
AlO2-+CO2+2H2O=Al(OH)3↓+HCO3-或2AlO2-+CO2+3H2O=2Al(OH)3↓+CO32-
AlO2-+CO2+2H2O=Al(OH)3↓+HCO3-或2AlO2-+CO2+3H2O=2Al(OH)3↓+CO32-
.