
题目列表(包括答案和解析)
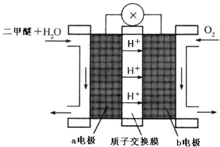


已知在1×105 Pa,298 K条件下,2 mol氢气燃烧生成水蒸气放出484 kJ热量,下列热化学方程式正确的是
A.H2O ( g ) = H2 ( g ) + 1/2O2 ( g ) △H = +242 kJ/mol
B.2H2 ( g ) + O2 ( g ) = 2H2O ( l ) △H = -484 kJ/mol
C.H2 ( g ) + 1/2O2 ( g ) = H2O ( g ) △H = +242 kJ/mo
D.2H2 ( g ) + O2 ( g ) = 2H2O ( g ) △H = +484 kJ/mol
能源短缺是人类面临的重大问题。甲醇是一种可再生能源,具有广泛的开发和应用前景。因此甲醇被称为21世纪的新型燃料。
(1)已知在常温常压下:
① 2CH3OH(l)+3O2(g)
2CO2(g)+4H2O(g) △H= -1275.6 kJ·mol—1
② H2O(l) H2O(g)
△H=+ 44.0 kJ.mo—1
写出表示甲醇燃烧热的热化学方程式 。
(2)工业上用CO生产燃料甲醇。一定条件下发生反应:CO(g)+2H2(g) CH3OH(g)。图1表示反应中能量的变化;图2表示一定温度下,在体积为2L的密闭容器中加入4mol H2和一定量的CO后,CO和CH3OH(g)的浓度随时间变化图。
CH3OH(g)。图1表示反应中能量的变化;图2表示一定温度下,在体积为2L的密闭容器中加入4mol H2和一定量的CO后,CO和CH3OH(g)的浓度随时间变化图。

①在“图1”中,曲线 (填“a”或“b”)表示使用了催化剂。
②能判断该反应在“图2”所在条件下是否已达化学平衡状态的依据是 。(双选)
A.容器中压强不变 B.体系的密度不随时间改变
C.v正(H2)=2v逆(CH3OH) D.CO与H2的物质的量的比不随时间改变
③计算该温度下CO(g)+2H2(g) CH3OH(g)的化学平衡常数K=
。
CH3OH(g)的化学平衡常数K=
。
④请在“图3”中画出平衡时甲醇百分含量(纵坐标)随温度(横坐标)变化的曲线,要求画压强不同的2条曲线(在曲线上标出P1、P2,且P1<P2)。
(3)CaSO4是一种微溶物质,已知Ksp(CaSO4)=9.10×10-6。现将c mol·L-1 CaCl2溶液与2.00×10-2 mol·L-1 Na2SO4溶液等体积混合生成沉淀,则c的最小值是 (结果保留3位有效数字)。
A.C(s)+![]() O2(g)=CO(g);ΔH =-y kJ·mol-1??
O2(g)=CO(g);ΔH =-y kJ·mol-1??
B.2C(s)+2O2(g)=2CO(g);ΔH =-x kJ·mol-1??
C.C(s)+![]() O2(g)=CO(g);ΔH =-(2x-y) kJ·mo-1??
O2(g)=CO(g);ΔH =-(2x-y) kJ·mo-1??
D.2C(s)+O2(g)=2CO(g);ΔH =-(2x-y) kJ·mol-1??
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com