
题目列表(包括答案和解析)
下图是不饱和烃加氢时能量变化示意图(E1代表反应物具有的总能量),具体数据如下:
| 反应 | ΔE |
| CH3C≡CCH3+2H2 | 278 kJ·mol-1 |
| CH2==CH—CH==CH2+2H2 | 239 kJ·mol-1 |

若化学反应总是向能量降低的方向进行,试分析判断下列问题:
(1)1 mol CH3CH2C≡CCH2CH2CH==CH—CH==CH2若与2 mol H2作用,其主要产物是_____________。
(2)如果CH3CHBrCHBrCH3与NaOH的醇溶液共热后,主要产物是A,则A的结构简式为___________,另一副产物是B。
(3)若反应(2)是吸热反应,试画出该反应中A与B的能量变化差异的示意图。

| T/K | 298 | 398 |
| 平衡常数K | K1 | K2 |
 能源是国民经济发展的重要基础,我国目前使用的能源主要是化石燃料.
能源是国民经济发展的重要基础,我国目前使用的能源主要是化石燃料. 氮是地球上含量丰富的一种元素,氮元素的单质和化合物在工农业生产、生活中有重要用途。
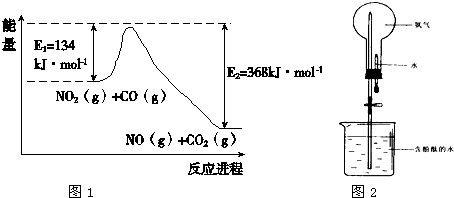
(1)根据右下能量变化示意图:

写出CO和NO2反应生成NO和CO2的热化学方程式
(2)在固定体积的密闭容器中,进行如下化学反应:N2(g)+3H2(g)  2NH3
(g) ΔH<0,
2NH3
(g) ΔH<0,
其平衡常数K与温度T的关系如下表,试判断K1 K2(填“>”、“=”或“<”)
|
T /K |
298 |
398 |
|
平衡常数K |
K1 |
K2 |
(3)下列各项能说明该反应达到平衡状态的是 (填字母序号)
a. v(H2)正=3 v(N2)逆
b. 容器内压强保持不变
c. 容器中混合气体的密度保持不变
d.: N2 、H2、NH3的浓度之比为1:3:2
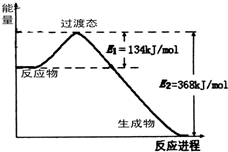
(4)氨气极易溶于水,常用下图实验来验证,在标准状况下,烧瓶中的氨水使酚酞变红。

请回答:
①用化学用语说明所得氨水能使酚酞变红的原因 。
②250C时,将一定量的氨水与盐酸混合后pH=7,测该混合溶液中c(Cl-)与c(NH4+)关系为 (填字母序号)
a.c(Cl-)﹥c(NH4+) b.c(Cl-)﹦c(NH4+)
c. c(Cl-)﹤c(NH4+) d.无法判断
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com