
题目列表(包括答案和解析)
高铁酸钾是一种高效的多功能水处理剂,具有氧化、吸附、絮凝、、助凝、杀菌、除臭等作用,高铁酸钾的开发和利用正日益显示出其广阔的应用前景。其制备流程如下:
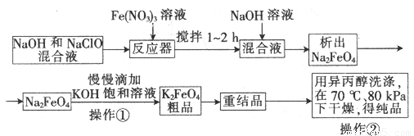
试回答下列问题
(1)反应器中,NaOH、NaClO、Fe(NO3)3发生反应生成Na2FeO4,完成并配平下列离子反应方程式:
□Fe3++□ClO─+□OH─ ==□FeO42─+□Cl─+□___________
(2)次氯酸钠浓度对高铁酸钾产率有一定影响,当NaClO浓度为298g/L时,高铁酸钠的产率最高,此时NaClO的物质的量浓度为_______________。
(3)你认为操作①能够发生转化的原因是__________,慢慢滴加的原因的是___________。
(4)操作②如果温度过高会造成高铁酸钾的分解,高铁酸钾受热分解时生成金属氧化物和氧气,该反应的化学方程式为__________________。
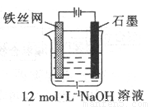
(5)可以用电化学法制取Na2FeO4,其装置如图所示,则阳极的电极反应式为 ;
阴极的电极反应式为______________;电解一段时间后溶OH─的浓度会_________(填“升高”、“降低”
或“不变”)。
______Fe(OH)3+______ClO-+_______OH-![]() ______
______![]() +_____Cl-+_______H2O
+_____Cl-+_______H2O
(2)已知有0.03 mol Fe(OH)3参加反应,共转移了5.4×1022个电子,则n=_________,![]() 中铁元素的化合价为_________。
中铁元素的化合价为_________。
(3)根据(1)(2)推测,![]() 能和下列_________(填序号)物质反应。
能和下列_________(填序号)物质反应。
A.KMnO4 B.SO
4CuI+Hg![]() Cu2HgI4+2Cu
Cu2HgI4+2Cu
(1)上述反应产物Cu2HgI4中,Cu元素显_______________价。
(2)以上反应中的氧化剂是__________,当有1 mol CuI参与反应时,转移电子________mol。
(3)CuI可由Cu2+和I-直接反应制得,配平下列离子反应方程式:□Cu2++□I-![]() □CuI+□
□CuI+□![]() 。
。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com