
题目列表(包括答案和解析)
卤族元素(9F、17Cl、35Br、53I、85At)是重要的非金属元素,它们的单质及其化合物不仅在无机化学中有极其广泛的应用,而且在有机化学中也表现不俗。请回答下列有关问题:
(1)指出氯元素在元素周期表中的位置 ;
(2)下列关于卤族元素的叙述不正确的是 (填字母);
A.卤素单质的颜色随原子序数的递增,由浅到深
B.卤化氢的沸点随原子序数的递增,由低到高
C.新制的氯水滴加到碘化钾溶液中,再滴加淀粉溶液呈蓝色,说明氯元素非金属性比碘强
D.氯化铁溶液中混有少量氯化亚铁,可滴加适量溴水除去
(3)利用你所学的有机反应,用化学方程式表示在有机化合物分子中引入卤素原子的方法
① 引入一个卤素原子,且属于取代反应: ;
② 引入两个卤素原子,且属于加成反应: ;
③ 引入四个卤素原子,且属于加成反应: 。
(4)海水中含有丰富的卤素,其中提取溴的一种工艺方法是在预先经过酸化的浓缩海水中通入氯气使溴离子转化成单质溴,继而通入空气和水蒸气,将溴吹入吸收塔,使溴蒸气和吸收剂SO2发生作用转化成氢溴酸以达到富集的目的。然后再用氯气将其氧化得到产品溴。
① 写出第二步转化的离子方程式: ;
② 用此法从海水中提取1mol溴单质,总共需要氯气 mol。
(5) 某校探究小组将少量粉末状硫磺撒到新制氯水中,充分振荡,硫磺粉消失,并检测到有两种强酸生成。写出该反应的化学方程式: 。
(18分) 三个课外实验小组用Na2SO3溶液、FeCl3溶液及其它试剂做了一系列实验:
第一组:烧瓶中盛装滴有酚酞的 Na2SO3溶液,并放置在盛有水的烧杯中,然后向烧杯中加入浓硫酸,实验过程中发现烧瓶中溶液红色_____(填“变深”、“变浅”或“不变”),下列有关叙述正确的是_________(填字母)。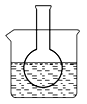
| A.溶液显浅红色是因为Na2SO3水解呈酸性 | B.水解反应为放热反应 |
| C.水解反应为吸热反应 | D.升高温度,Na2SO3水解程度增大 |
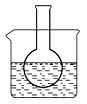
| A.溶液显浅红色是因为Na2SO3水解呈酸性 | B.水解反应为放热反应 |
| C.水解反应为吸热反应 | D.升高温度,Na2SO3水解程度增大 |
化学是一门以实验为基础的自然科学,化学实验在化学学习中具有极其重要的作用。
(1) 下列关于实验的叙述正确的有_______________________。
A.燃着的酒精灯不慎碰翻失火,应立即用湿布盖灭
B.滴定实验中用的移液管、锥形瓶和滴定管都要用所盛溶液润洗
C.做完酚醛树脂实验的试管可用乙醇浸泡后清洗。
D.酸性高锰酸钾溶液一般用盐酸酸化,可除去乙烯中混有的二氧化硫气体
E.除去氯化镁溶液中含有的FeCl3 杂质, 可采用加入MgO调节pH除去。
F.蒸发操作时,用玻璃棒不断搅拌,防止液体飞溅出来,等水分完全蒸干后,停止加热
G.可用移液管量取0.10 mol/L 的KMnO4溶液25.10 mL
H. 用pH试纸测得某新制氯水的pH值为3
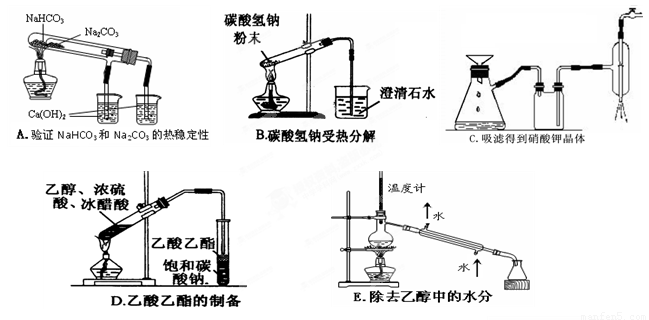 (2 ) 下列实验没有错误的是_______________________
(2 ) 下列实验没有错误的是_______________________
(3) 下图为常见仪器的部分结构(有的仪器被放大)
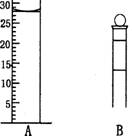
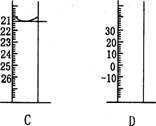
A图中液面所示溶液的体积为__________mL,用上述四种仪器中的某种测量一液体的体积, 平视时读数为NmL,仰视时读数为M mL,若M>N,则所使用的仪器是________(填字母标号)。
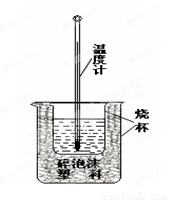
(4).中和热的测定如右图所示,该装置图中有两处实验用品没有画出,它们是烧杯上方的泡沫塑料盖和_________________。完成一次中和热测定实验,温度计至少要使用 次。
化学是一门以实验为基础的自然科学,化学实验在化学学习中具有极其重要的作用。
(1) 下列关于实验的叙述正确的有_______________________。
A.燃着的酒精灯不慎碰翻失火,应立即用湿布盖灭
B.滴定实验中用的移液管、锥形瓶和滴定管都要用所盛溶液润洗
C.做完酚醛树脂实验的试管可用乙醇浸泡后清洗。
D.酸性高锰酸钾溶液一般用盐酸酸化,可除去乙烯中混有的二氧化硫气体
E.除去氯化镁溶液中含有的FeCl3 杂质, 可采用加入MgO调节pH除去。
F.蒸发操作时,用玻璃棒不断搅拌,防止液体飞溅出来,等水分完全蒸干后,停止加热
G.可用移液管量取0.10 mol/L 的KMnO4溶液25.10 mL
H. 用pH试纸测得某新制氯水的pH值为3
(2 ) 下列实验没有错误的是_______________________
(3) 下图为常见仪器的部分结构(有的仪器被放大)
A图中液面所示溶液的体积为__________mL,用上述四种仪器中的某种测量一液体的体积, 平视时读数为NmL,仰视时读数为M mL,若M>N,则所使用的仪器是________(填字母标号)。
(4).中和热的测定如右图所示,该装置图中有两处实验用品没有画出,它们是烧杯上方的泡沫塑料盖和_________________。完成一次中和热测定实验,温度计至少要使用 次。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com