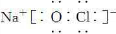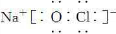下表为元素周期表的一部分,请回答有关问题:
族
周期 |
ⅠA |
ⅡA |
ⅢA |
ⅣA |
ⅤA |
ⅥA |
ⅦA |
0 |
| 2 |
|
|
|
① |
② |
|
③ |
|
| 3 |
|
④ |
⑤ |
⑥ |
|
⑦ |
⑧ |
⑨ |
| 4 |
⑩ |
|
|
|
|
|
(11) |
|
(1)表中化学性质最不活泼的元素,其原子结构示意简图为
;
(2)表中能形成两性氢氧化物的元素是
Al
Al
(用元素符号表示),写出该氢氧化物与⑩的最高正价氧化物对应水化物反应的化学方程式
Al(OH)3+KOH=KAlO2+2H2O
Al(OH)3+KOH=KAlO2+2H2O
;
(3)①、②、⑦、⑧四种元素的最高价氧化物对应水化物中酸性最强的是
HClO4
HClO4
(用化学式表示);
(4)③元素和(11)元素两者的核电荷数之差是
26
26
;
(5)④、⑤两元素相比较,金属性较强的是
镁
镁
(填名称),可以验证该实验结论的实验是
B C
B C
.
A.将在空气中放置已久的这两种元素的块状单质分别放入热水中
B.将形状、大小相同的这两种元素的单质分别和同浓度的盐酸反应
C.将形状、大小相同的这两种元素的单质分别和热水作用,并滴入酚酞溶液
D.比较这两种元素气态氢化物的稳定性
(6)高性能的现代通讯材料--光导纤维是
⑥
⑥
(填编号)的氧化物制造出来的.写出该氧化物和氢氧化钠溶液反应的化学方程式
SiO2+2NaOH═Na2SiO3+H2O
SiO2+2NaOH═Na2SiO3+H2O
.
(7)③与⑩能形成
离子
离子
(填:“离子”或“共价”)化合物.
(8)⑩的单质与水反应的化学方程式
2K+2H2O=2KOH+H2↑
2K+2H2O=2KOH+H2↑
.
用洁净的铂丝棒蘸取上述反应后的溶液在酒精灯上灼烧,能够观察到
紫
紫
色火焰.






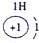
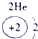
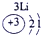
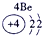
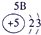
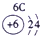
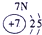
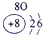
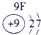
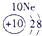
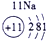





 表示的是
表示的是