
题目列表(包括答案和解析)
| 13 |
| 2 |
| 13 |
| 2 |
| 9 |
| 2 |
| 9 |
| 2 |
| 13 |
| 2 |
| 13 |
| 2 |
| 9 |
| 2 |
| 9 |
| 2 |
| 13 |
| 2 |
| 13 |
| 2 |
| 9 |
| 2 |
| A、2878kJ/mol |
| B、2658kJ/mol |
| C、1746kJ/mol |
| D、5756kJ/mol |
下面均是正丁烷与氧气反应的热化学方程式(25°,101kPa):
①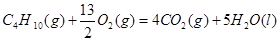

②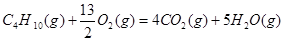
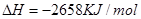
③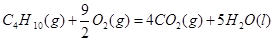

④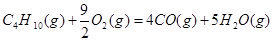
由此判断,正丁烷的燃烧热是
A.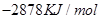 B.
B.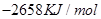 C.
C.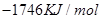 D.
D.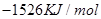
下面均是正丁烷与氧气反应的热化学方程式(25°,101kPa):
①C4H10(g)+  O2(g)=4CO2(g)+5H2O(l)
ΔH=-2878kJ/mol
O2(g)=4CO2(g)+5H2O(l)
ΔH=-2878kJ/mol
②C4H10(g)+ 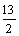 O2(g)=4CO2(g)+5H2O(g)
ΔH=-2658kJ/mol
O2(g)=4CO2(g)+5H2O(g)
ΔH=-2658kJ/mol
③C4H10(g)+ 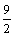 O2(g)=4CO(g)+5H2O(l)
ΔH=-1746kJ/mol
O2(g)=4CO(g)+5H2O(l)
ΔH=-1746kJ/mol
④C4H10(g)+ 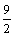 O2(g)=4CO(g)+5H2O(g)
ΔH=-1526kJ/mol
O2(g)=4CO(g)+5H2O(g)
ΔH=-1526kJ/mol
由此判断,正丁烷的燃烧热是
A.-2878kJ/mol B. -2658kJ/mol
C.+1746kJ/mol D. -1526 kJ/mo
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com