
题目列表(包括答案和解析)
已知2SO2+O2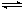 2SO3; △H=-92.6 kJ·mol-1,当反应达到平衡时,下列措施:①降低温度;②减小压强;③用V2O5作催化剂;④增大O2的浓度;⑤增大SO2的浓度;⑥恒压通入He气,能提高SO2转化率的是
2SO3; △H=-92.6 kJ·mol-1,当反应达到平衡时,下列措施:①降低温度;②减小压强;③用V2O5作催化剂;④增大O2的浓度;⑤增大SO2的浓度;⑥恒压通入He气,能提高SO2转化率的是
A.①②⑥ B.①④⑤ C.④⑤⑥ D.①④
已知2SO2+O2![]() 2SO3; △H=-92.6 kJ·mol-1,当反应达到平衡时,下列措施:①降低温度;②减小压强;③用V2O5作催化剂;④增大O2的浓度;⑤增大SO2的浓度;⑥恒压通入He气,能提高SO2转化率的是
2SO3; △H=-92.6 kJ·mol-1,当反应达到平衡时,下列措施:①降低温度;②减小压强;③用V2O5作催化剂;④增大O2的浓度;⑤增大SO2的浓度;⑥恒压通入He气,能提高SO2转化率的是
A.①②⑥ B.①④⑤ C.④⑤⑥ D.①④
已知2SO2+O22SO3; △H=-92.6 kJ·mol-1,当反应达到平衡时,下列措施:①降低温度;②减小压强;③用V2O5作催化剂;④增大O2的浓度;⑤增大SO2的浓度;⑥恒压通入He气,能提高SO2转化率的是
A.①②⑥ B.①④⑤ C.④⑤⑥ D.①④
已知2SO2+O2 2SO3;△H=-92.6 kJ·mol-1,当反应达到平衡时,下列措施:①降低温度;②减小压强;③用V2O5作催化剂;④增大O2的浓度;⑤增大SO2的浓度;⑥恒压通入He气,能提高SO2转化率的是
2SO3;△H=-92.6 kJ·mol-1,当反应达到平衡时,下列措施:①降低温度;②减小压强;③用V2O5作催化剂;④增大O2的浓度;⑤增大SO2的浓度;⑥恒压通入He气,能提高SO2转化率的是
| A.①②⑥ | B.①④⑤ | C.④⑤⑥ | D.①④ |
水体中二价汞离子可以与多种阴离子结合成不同的存在形态.水溶液中二价汞主要存在形态与Cl-、OH-的浓度关系如图所示:

(1)正常海水(Cl-的浓度大于0.1 mol/L)中汞元素的主要存在形态是________.少量Hg(NO3)2溶于0.001 mol/L的盐酸后得到无色透明溶液,其中汞元素的主要存在形态是________.
(2)Hg(NO3)2固体易溶于水,但溶于水时常常会出现浑浊,其原因是________(用离子方程式表示),为了防止出现浑浊,可采取的措施是________.
(3)处理含汞废水的方法很多.下面是常用的两种方法,汞的回收率很高.
①置换法:用废铜屑处理含Hg2+的废水.反应的离子方程式为________.
②化学沉淀法:用硫化钠处理含Hg(NO3)2的废水,生成HgS沉淀.已知:
Ksp(HgS)=1.6
×10-52,当废水中c(S2-)=1×10-5 mol/L时,c(Hg2+)=________.③用难溶的FeS作为沉淀剂也可使Hg2+转化为HgS而除去,该反应的离子方程式:________.有人认为加入FeS作为沉淀剂还可以起到净化水的作用,请运用所学知识解释________
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com