
题目列表(包括答案和解析)
| 编号 | 实验内容 | 实验原理 | 气体发生装置 |
| ① | 制备氧气 | H2O2→O2 | Ⅳ Ⅳ |
| ② | 制备氨气 | NH4Cl→NH3 | Ⅱ Ⅱ |
| ③ | 制备氯气 | HCl→Cl2 | Ⅰ或Ⅳ Ⅰ或Ⅳ |



已知①~④均为工业生产及应用的常见反应。其中常温下B、D、J、P气体,E为分子中原子个数比为1∶l的液体。A的相对分子质量为120。(个别反应的产物已略去)
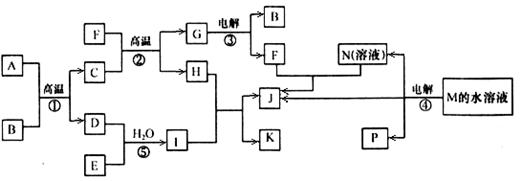
试回答下列问题:
(1)反应F与N溶液反应的离子方程式为________________________________________;
(2)反应⑤中当有1mol电子转移时,氧化剂消耗 g。
(3)反应④的离子方程式为______________________________;
右图是该反应原理的示意图,该装置中使用的是 (填“阴”或“阳”)离子交换膜。图中从d处收集到的是 。
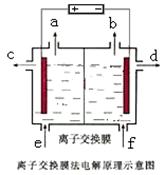
(4)工业上由D制取I的过程可表示为:
![]()
由D与B反应生成X的反应所用的设备是
①高炉 ②沸腾炉 ③接触室 ④分馏塔 ⑤吸收塔
已知400℃ 101Kpa时,2D(g) + B(g)![]() 2X(g);△H = – 196.6KJ/mol,当2 mol D与1 mol B在该条件下反应达平衡时反应放热186.8 KJ。
2X(g);△H = – 196.6KJ/mol,当2 mol D与1 mol B在该条件下反应达平衡时反应放热186.8 KJ。
在实际生产中综合考虑各种因素,为提高D的转化率,工业选择了以下哪些条件______
①适当升高温度 ②增大压强 ③使用合适的催化剂 ④及时移走生成物 ⑤适当增大B的浓度 ⑥将反应物与生成物在热交换器中进行热交换
(15分) 已知①~④均为工业生产及应用的常见反应。其中常温下B、D、J、P气体,E为分子中原子个数比为1∶l的液体。A的相对分子质量为120。(个别反应的产物已略去)
试回答下列问题:
(1)反应F与N溶液反应的离子方程式为________________________________________;
(2)反应⑤中当有1mol电子转移时,氧化剂消耗 g。
(3)反应④的离子方程式为______________________________;
右图是该反应原理的示意图,该装置中使用的是 (填“阴”或“阳”)离子交换膜。图中从d处收集到的是 。
(4)工业上由D制取I的过程可表示为:
由D与B反应生成X的反应所用的设备是
①高炉 ②沸腾炉 ③接触室 ④分馏塔 ⑤吸收塔
已知400℃ 101Kpa时,2D(g) + B(g)![]() 2X(g);△H = – 196.6KJ/mol,当2 mol D与1mol B在该条件下反应达平衡时反应放热186.8 KJ。
2X(g);△H = – 196.6KJ/mol,当2 mol D与1mol B在该条件下反应达平衡时反应放热186.8 KJ。
在实际生产中综合考虑各种因素,为提高D的转化率,工业选择了以下哪些条件______
①适当升高温度 ②增大压强 ③使用合适的催化剂 ④及时移走生成物 ⑤适当增大B的浓度 ⑥将反应物与生成物在热交换器中进行热交换
(15分) 已知①~④均为工业生产及应用的常见反应。其中常温下B、D、J、P气体,E为分子中原子个数比为1∶l的液体。A的相对分子质量为120。(个别反应的产物已略去)
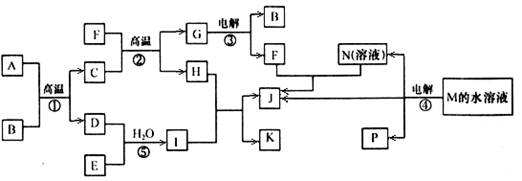
试回答下列问题:
(1)反应F与N溶液反应的离子方程式为________________________________________;
(2)反应⑤中当有1mol电子转移时,氧化剂消耗 g。
(3)反应④的离子方程式为______________________________;
右图是该反应原理的示意图,该装置中使用的是 (填“阴”或“阳”)离子交换膜。图中从d处收集到的是 。
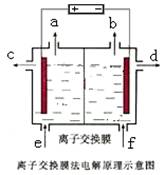
(4)工业上由D制取I的过程可表示为:
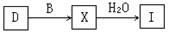
由D与B反应生成X的反应所用的设备是
①高炉 ②沸腾炉 ③接触室 ④分馏塔 ⑤吸收塔
已知400℃ 101Kpa时,2D(g) + B(g) 2X(g);△H = – 196.6KJ/mol,当2 mol D与1
mol B在该条件下反应达平衡时反应放热186.8 KJ。
2X(g);△H = – 196.6KJ/mol,当2 mol D与1
mol B在该条件下反应达平衡时反应放热186.8 KJ。
在实际生产中综合考虑各种因素,为提高D的转化率,工业选择了以下哪些条件______
①适当升高温度 ②增大压强 ③使用合适的催化剂 ④及时移走生成物 ⑤适当增大B的浓度 ⑥将反应物与生成物在热交换器中进行热交换
实验室模拟合成氨和氨催化氧化的流程如下:
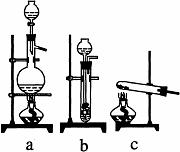
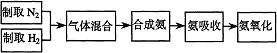
已知实验室可用饱和亚硝酸钠(NaNO2)溶液与饱和氯化铵溶液经加热后反应制取氮气。
(1)从右图中选择制取气体的合适装置:氮气 、氢气 。
(2)氮气和氢气通过甲装置,甲装置的作用除了将气体混合外,还有 、 。
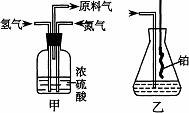
(3)氨合成器出来经冷却的气体连续通入乙装置的水中吸收氨, (“会”或“不会”)发生倒吸,原因是: 。
(4)用乙装置吸收一段时间氨后,再通入空气,同时将经加热的铂丝插入乙装置的锥形瓶内,能使铂丝保持红热的原因是: ,锥形瓶中还可观察到的现象是: 。
(5)写出乙装置中氨氧化的化学方程式:
(6)反应结束后锥形瓶内的溶液中含有H+、OH-、 、 离子。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com