
题目列表(包括答案和解析)
盐酸是应用广泛的酸之一,它具有:①酸性 ②氧化性 ③还原性 ④挥发性。请回答下列问题:
(1)浓盐酸长时间露置在空气中,溶液的质量减轻表现了____________(填序号)。
(2)实验室用稀盐酸和锌粒反应制取氢气表现了____________(填序号),反应的离子方程式为- 。
(3)用盐酸除去铁表面的铁锈表现了____________(填序号),反应的离子方程式为_________________。
(4)实验室常用KMnO4和浓盐酸反应制取Cl2,反应的方程式为2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O。
①被还原的元素是____________,还原剂是____________。
②氧化产物是____________,若生成5 mol Cl2,转移的电子总数为____________。
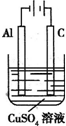 金属铝是应用广泛的金属之一,在工农业生产中有着广泛的应用,对金属制品进行抗腐蚀处理,可延长其使用寿命.
金属铝是应用广泛的金属之一,在工农业生产中有着广泛的应用,对金属制品进行抗腐蚀处理,可延长其使用寿命.目前世界各国获得镁的主要来源 从海水中提取,以下是提取镁的过程中涉及到的几种物质常温下的溶度积常数,根据你所学的知识回答下面的几个问题:?
从海水中提取,以下是提取镁的过程中涉及到的几种物质常温下的溶度积常数,根据你所学的知识回答下面的几个问题:?
| 物质 | CaCO3 | MgCO3 | Ca(OH)2 | Mg(OH)2 |
| 溶度积 | 2.8×10-9 | 6.8×10-6 | 5.5×10-6 | 1.8×10-11 |
目前世界各国获得镁的主要来源从海水中提取,以下是提取镁的过程中涉及到的几种物质常温下的溶度积常数,根据你所学的知识回答下面的几个问题:?
|
物质 |
CaCO3 |
MgCO3 |
Ca(OH)2 |
Mg(OH)2 |
|
溶度积 |
2.8×10-9 |
6.8×10-6 |
5.5×10-6 |
1.8×10-11 |
(1)在从海水中提取镁时,往往用到贝壳(主要成分是CaCO3),你认为 (填“能”或“不能”)通过将贝壳研磨成粉末直接投入海水里制备含镁的沉淀,理由是 。如果不能直接投入,应将贝壳作何处理,试写出化学方程式: 。(若第一个空格填“能”,此空格不填;若填“不能”, 此空格只须第一步处理的化学反应方程式。)
(2)已知某地海水中的镁离子的浓度为1.8×10-3 mol·L-1,则常温下要使镁离子产生沉淀,溶液pH最低应为 。
(3)实验室中常用CaCO3制CO2,其产物之一的氯化钙是应用广泛的化学试剂,可作干燥剂、冷冻剂等。为了测定某氯化钙样品中钙元素的含量,进行如下实验:
(I)准确称取氯化钙样品0.2000g,放入烧杯中,加入适量6mol/L的盐酸和适量蒸馏水使样品完全溶解,再加入35mL 0.25mol/L (NH4)2C2O4溶液,水浴加热,逐渐生成CaC2O4沉淀,经检验,Ca2+已沉淀完全。
(II)过滤并洗涤(I)所得沉淀。
(III)加入足量的10% H2SO4溶液和适量的蒸馏水,(II)中沉淀完全溶解,溶液呈酸性,加热至75℃,趁热逐滴加入0.05000 mol/L KMnO4溶液16.00mL,恰好完全反应。请回答:
已知滴定过程发生的反应为2MnO4- + 5H2C2O4 + 6H+ ="=2" Mn2+ +10 CO2↑+8 H2O(已配平)
①0.05000 mol/L KMnO4溶液标准溶液应置于 (选填“酸式”或“碱式”)滴定管中。
②滴定终点的现象为 。
③该氯化钙样品中钙元素的质量百分数为 。
目前世界各国获得镁的主要来源从海水中提取,以下是提取镁的过程中涉及到的几种物质常温下的溶度积常数,根据你所学的知识回答下面的几个问题:
| 物质 | CaCO3 | MgCO3 | Ca(OH)2 | Mg(OH)2 |
| 溶度积 | 2.8×10-9 | 6.8×10-6 | 5.5×10-6 | 1.8×10-11 |
(1)在从海水中提取镁时,往往用到贝壳(主要成分是CaCO3),你认为 (填“能”或“不能”)通过将贝壳研磨成粉末直接投入海水里制备含镁的沉淀,理由是 。如果不能直接投入,应将贝壳作何处理,试写出化学方程式: 。(若第一个空格填“能”,此空格不填;若填“不能”, 此空格只须第一步处理的化学反应方程式。)
(2)已知某地海水中的镁离子的浓度为1.8×10-3 mol·L-1,则常温下要使镁离子产生沉淀,溶液pH最低应为 。
(3)实验室中常用CaCO3制CO2,其产物之一的氯化钙是应用广泛的化学试剂,可作干燥剂、冷冻剂等。为了测定某氯化钙样品中钙元素的含量,进行如下实验:
(I)准确称取氯化钙样品0.2000g,放入烧杯中,加入适量6mol/L的盐酸和适量蒸馏水使样品完全溶解,再加入35mL 0.25mol/L (NH4)2C2O4溶液,水浴加热,逐渐生成CaC2O4沉淀,经检验,Ca2+已沉淀完全。
(II)过滤并洗涤(I)所得沉淀。
(III)加入足量的10% H2SO4溶液和适量的蒸馏水,(II)中沉淀完全溶解,溶液呈酸性,加热至75℃,趁热逐滴加入0.05000 mol/L KMnO4溶液16.00mL,恰好完全反应。请回答:
已知滴定过程发生的反应为2MnO4- + 5H2C2O4 + 6H+ ==2 Mn2+ +10 CO2↑+8 H2O(已配平)
①0.05000 mol/L KMnO4溶液标准溶液应置于 (选填“酸式”或“碱式”)滴定管中。
②滴定终点的现象为 。
③该氯化钙样品中钙元素的质量百分数为 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com