
题目列表(包括答案和解析)
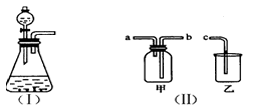
下图(I)是实验室制取气体的一种发生装置。
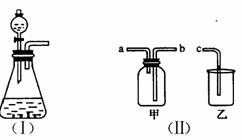
(1)若用上述装置制取O2,可选择二氧化锰和 反应,写出此反应的化学方程式 。
(2)选择图(II)中的甲装置,若用排空气法收集CO2,收集时气体应从 口进气;若用排水法收集O2,收集时气体应从 口进气。(填“a”或“b”)
(3)实验室以KMnO4和浓盐酸为反应物,利用(I)、(II)装置组合制取氯气,反应方程式如下:
□KMnO4+□HCl=□KCl+□MnCl2+□Cl2↑+□H2O
①配平上述反应方程式(在空格里填上适合的计量系数);
盐酸在此反应中体现的性质为
②组合装置乙中盛放氢氧化钠溶液,发生反应的离子方程式为 。
(4)广口瓶被称为气体实验的“万能瓶”,是因为它可以配合玻璃管和其他简单仪器组成各种用途的装置。如充当集气瓶,还可作 (填写一种即可)
I. 实验室里用二氧化锰和浓盐酸加热制取氯气,该反应的离子方程式为: MnO2+4H++2Cl—![]() Mn2++Cl2↑+2H2O,也可以利用反应:
Mn2++Cl2↑+2H2O,也可以利用反应:
2KMnO4+16HCl(浓) 2KCl+2MnCl2+5Cl2↑+8H2O制取并收集纯净、干燥的氯气,部分装置如图所示:
|
(1)若以KMnO4和浓盐酸为原料制取氯气,请根据反应原理从下图中选择合适的制气装置 (填代号)。
|
(2)装置B的作用是 。
(3)E中的试剂可选用 (填代号)。
A.NaOH溶液 B.Na2CO3溶液 C.NaCl溶液 D.水
(4)某学生通过下列两种方式制取氯气:
①用8.7gMnO2与足量浓盐酸反应制取Cl2
②用含14.6gHCl的浓盐酸与足量MnO2反应制取Cl2
这两种方式产生Cl2的量的关系是 。
A.①多 B.②多 C.①②一样多
II.现欲用碳酸钙固体和稀盐酸反应制取CO2气体,请回答下列问题:
(1)写出发生反应的离子方程式 ;
|
[V(CO2)]与时间(t)的关系如图
所示,试分析判断OE段、EF段、
FG段反应速率[分别用![]() (OE)、
(OE)、![]()
(EF)、![]() (FG)表示]的大小关系
(FG)表示]的大小关系
;比较OE段和EF
段,说明EF段速率变化的主要原因
应该是 。

①设计甲装置的目的是_________________。甲装置__________(填“能”或“不能”)用乙装置来代替。
②装置乙中盛有的液体是__________,该装置可看作是一个___________(填某仪器名称)。
(2)在氮的化合物中,有一类盐叫亚硝酸盐,如亚硝酸钠(NaNO2)等。NaNO2是一种潜在的致癌物质,过量或长期使用会对人产生危害。由于亚硝酸钠有咸味,外观与NaCl相似,曾多次发生过被误当食盐使用的事件。已知:HNO2是一种弱酸,不稳定,易分解生成NO和NO2;它能被常见的强氧化剂氧化;在酸性溶液中它也是一种氧化剂,如能把I-氧化成I2;AgNO2是一种难溶于水易溶于酸的化合物。试回答下列问题:
①人体正常的血红蛋白中应含Fe2+。若误食亚硝酸盐(如NaNO2),则导致血红蛋白中Fe2+转化为Fe3+而中毒,服用维生素C可解毒。下列叙述不正确的是_____________。
A.亚硝酸盐是还原剂 B.维生素C是还原剂
C.维生素C将Fe3+还原为Fe2+ D.亚硝酸盐被还原
②下列说法中,能用来区别NaNO2和NaCl的是______________。
A.测定这两种溶液的pH
B.用AgNO3和HNO3两种试剂来区别
C.在酸性条件下加入KI淀粉试液来区别
③把新制氯气通入到NaNO2溶液中,氯水褪色,生成NaNO3和HCl,请写出此反应的离子方程式______________。
④为了测定某样品中NaNO2的含量,可以使用标准?KMnO4?溶液进行滴定,试回答:KMnO4溶液在滴定过程中作____________(填“氧化剂”或“还原剂”),该滴定过程_____________(填“要”或“不要”)另加指示剂。
⑤已知HNO2的酸性比醋酸略强,某同学在家中进行鉴别NaNO2与NaCl的实验,但他家中只有浓醋酸,请问该实验能否成功?____________(填“能”或“不能”),请说明理由_______
_____________________________________________________________________。
下面是一些实验室制备硫酸铜的实验设计。
实验一:用铜与浓硫酸反应制取硫酸铜。
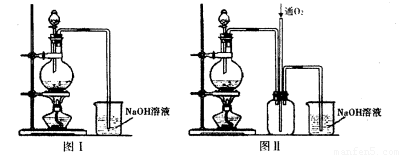
实验二:将适量浓硝酸分多次加入到铜粉与稀硫酸的混合物中,加热使之反应完全制取硫酸铜。(装置如下图中的图I.图Ⅱ)。
实验三:将铜粉在某仪器中反复灼烧,使铜粉充分与空气发生反应生成氧化铜,再将氧化铜与稀硫酸反应,经后续步骤可得到硫酸铜晶体。
实验四:向铜粉和稀硫酸的混合物中加入H2O得到硫酸铜。
请回答实验中的有关问题。
(1)实验一中发生反应的化学反应方程式为____,这种方法的缺点是____。
(2)实验二装置图中分液漏斗里盛装的液体是____。图Ⅱ是图I的改进装置,分析图II装置的优点是 。
(3)实验三中用于灼烧的仪器名称是 。该实验中的后续步骤指的是__ 。
(4)实验四中发生反应的化学方程式为____。
(5)除上面的实验设计外,请你再设计一种只用铜和稀硫酸为原料制取硫酸铜的方法(写出化学反应方程式)。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com