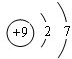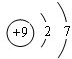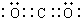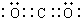A、B、C、D、E是常见化合物或单质,有如下转化关系(略去条件和副产品).
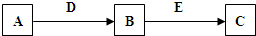
(1)若D为氧气,C为NaAlO
2,试写出B转化为C的化学方程式
Al2O3+2NaOH=2NaAlO2+H2O
Al2O3+2NaOH=2NaAlO2+H2O
.
(2)若A为气态单质,B为漂白粉的有效成份,C具有漂白性.试写A转化为B的化学方程式
2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O
2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O
.画出组成单质A的元素原子结构示意图.
(3)若A、B、C均为钠盐的水溶液,D、E均为卤素单质,请写出B转化为C的离子方程式
2Br-+Cl2=Br2+2Cl-
2Br-+Cl2=Br2+2Cl-
.
(4)若A常温下为固态单质,化合物B在常温常压下为气体,B和C的相对分子质量之比为4:5,且D、E为同一物质,则B为
SO2
SO2
.
(5)若B、D为质子数小于18的元素原子形成的单质,A、E、C均为氧化物,且D所含元素原子的质子数是B的2倍,A转化为B,B转化为C两个反应均属置换反应,请写出A转化为B的化学方程式
.


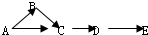 其中A是单质,B是气体,C、D是氧化物,E是最高价氧化物对应的水化物.
其中A是单质,B是气体,C、D是氧化物,E是最高价氧化物对应的水化物.