
题目列表(包括答案和解析)
亚铁是血红蛋白的重要组成成分,人如果缺铁就可能出现缺铁性贫血。下面是一种补铁药品说明书中的部分内容:该药品为无水碱式盐,含Fe2+34%~36%,是薄衣片……与Vc(维生素C)同服可增加本品吸收。
某同学设计实验对其中的铁成分进行了验证,请一起完成该实验。
(1)查阅资料得知,双氧水既可以氧化SCN-生成N2、CO2和SO![]() ,也可以将Fe2+氧化成Fe3+。
,也可以将Fe2+氧化成Fe3+。
(2)向去掉糖衣、研磨好的药品中加稀盐酸,得到浅绿色浑浊液,说明有______(填离子符号)存在。
(3)往上述溶液中滴入几滴KSCN溶液,出现浅红色,说明溶液中有少量Fe3+存在。该离子存在的原因可能是________(填字母)。
a.药品中的铁本来就是以三价铁的形式存在
b.在制药过程中生成少量三价铁
c.本实验过程中有少量二价铁被氧化为三价铁
(4)将(3)中所得溶液分成2份,分别装在A、B 2支试管中。
(5)向A试管的溶液中加入少量稀硫酸,再慢慢滴入过量的H2O2溶液,溶液的红色先变深,之后红色逐渐褪去。红色变深的原因是____________________________________________(用离子方程式表示)。
(6)向B试管的溶液中加入一片Vc片,片刻后溶液红色也褪去,说明Vc有________性。
亚铁是血红蛋白的重要组成成分,起着向人体组织传送O2 的作用,若缺铁就可能出现缺铁性贫血。下面是一种常见补铁药品说明书中的部分内容:该药品含Fe2+ 33%—36%,不溶于水但能溶于人体中的胃酸;与Vc(维生素C)同服可增加本品吸收。
Ⅰ.甲同学设计了以下实验检测该补铁药品中是否含有Fe2+并探究Vc的作用:
![]()
⑴加入新制氯水后溶液中发生的离子反应方程式是_____________、 。
⑵加入KSCN后溶液变淡红色,说明溶液中有少量Fe3+。该离子存在的可能原因___________。
A.药品中的铁本来就应该以三价铁的形式存在
B.在实验过程中有少量二价铁被氧化 C.药品储存过程中有少量三价铁生成
⑶向血红色溶液中加入一片Vc片,片刻后溶液血红色褪去,说明Vc有 性。
Ⅱ.乙同学采用酸性高锰酸钾标准液滴定法测定该药品是否合格,原理:5Fe2++8H++MnO4-=5Fe3++2Mn2++4H2O 。准确称量上述药品10.00g,将其全部溶于试剂2,配成1000mL溶液,取出20.00mL,用0.0200 mol·L-1的KMnO4 溶液滴定,用去KMnO4溶液12.00 mL.
⑷该实验中的试剂2与甲同学设计实验中的试剂1都可以是 (填编号)。
A.蒸馏水 B.稀盐酸 C.稀硫酸 D.稀硝酸
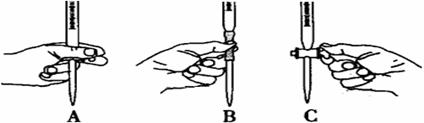
⑸本实验滴定过程中操作滴定管的图示正确的是 (填编号)。
⑹判断实验到达滴定终点的现象为 。
(7)经计算该药品中铁元素的百分含量为 。
亚铁是血红蛋白的重要组成成分,起着向人体组织传送O2的作用,人如果缺铁就可能出现缺铁性贫血,但是摄入过量的铁也有害.下面是一种补铁药品说明书中的部分内容:该药品为无水碱式盐,含Fe2+34%~36%,是薄衣片,……,与VC(维生素C)同服可增加本品吸收.
某同学设计实验对其中的铁成分进行了验证.请一起完成该实验:
第一步:查阅资料得知,双氧水可以氧化SCN-生成N2、CO2和SO42-,也可以将Fe2+氧化成Fe3+.
第二步:向去掉糖衣、研磨好的药品中加稀盐酸,出现淡绿色浑浊液,说明有________离子存在(填离子符号);
第三步:往上述溶液中滴入几滴KSCN溶液,出现浅红色,说明溶液中有少量Fe3+离子存在.该离子存在的原因可能是(填序号):________
①药品中的铁本来就是以三价铁的形式存在;②在制药过程中生成少量三价铁;③本实验过程中有少量三价铁生成.
第四步:将第三步所得溶液分成2份,分别装在A、B两个试管中.
第五步:向A试管的溶液中加入少量稀硫酸,再慢慢滴入过量的H2O2溶液,溶液的红色先变深,之后红色逐渐褪去.
红色变深的原因是(用离子方程式表示):________;
溶液红色又褪去的原因可能是:________;
请自选中学实验室中常用仪器、药品,设计实验证明你的推测:________;
第六步:向B试管的溶液中加入一片VC片,片刻后溶液红色也褪去,说明VC有________性;怎样理解药品说明中所述“与VC同服可增加本品吸收”这句话?________.
(14分)亚铁是血红蛋白的重要组成部分,起着向人体组织传送O2的作用,人如果缺铁就可能出现缺铁性贫。下面是一种补铁药品说明书中的部分内容:该药品为无水碱式盐,含Fe2+34%~36%,是薄衣片,与VC(维生素C)同服可增加本品吸收。某同学设计实验对其中的铁成分进行了验证。请一起完成实验:
第一步:查阅资料得知,双氧水可以氧化SCN—生成N2、CO2、和SO42—,也可以将Fe2+ 氧化成 Fe3+。
第二步:向去掉糖衣、研磨好的药品中加稀盐酸,出现淡绿色混浊液,说明有 存在(填离子符号)。
第三步:往上述溶液中滴入几滴KSCN溶液出现浅红色,说明溶液中有少量Fe3+存在。该离子存在的原因可能是(填序号):
①药品中的铁本来就以Fe3+的形式存在:②在制药过程中生成少量Fe3+;
②本实验过程中有少量Fe3+生成。
第四步:将第三步所得溶液分成两份,分别装在A、B两个试管中。
第五步:向A试管的溶液中加入少量稀硫酸,再慢慢滴入过量的H2O2溶液,溶液的红色先变深,之后红色逐渐褪去。
红色变深的原因是(用离子方程式表示) 红色又逐渐褪去的原因可能是
设计实验证明你的推测
第六步:向B试管的溶液中加入一片VC,片刻后溶液红色也褪去,说明VC有 性。怎样理解药品说明书中所述“与VC(维生素C)同服可增加本品吸收”这句话?
。
(14分)亚铁是血红蛋白的重要组成部分,起着向人体组织传送O2的作用,人如果缺铁就可能出现缺铁性贫。下面是一种补铁药品说明书中的部分内容:该药品为无水碱式盐,含Fe2+34%~36%,是薄衣片,与VC(维生素C)同服可增加本品吸收。某同学设计实验对其中的铁成分进行了验证。请一起完成实验:
第一步:查阅资料得知,双氧水可以氧化SCN—生成N2、CO2、和SO42—,也可以将Fe2+氧化成 Fe3+。
第二步:向去掉糖衣、研磨好的药品中加稀盐酸,出现淡绿色混浊液,说明有 存在(填离子符号)。
第三步:往上述溶液中滴入几滴KSCN溶液出现浅红色,说明溶液中有少量Fe3+存在。该离子存在的原因可能是(填序号):
①药品中的铁本来就以Fe3+的形式存在:②在制药过程中生成少量Fe3+;
②本实验过程中有少量Fe3+生成。
第四步:将第三步所得溶液分成两份,分别装在A、B两个试管中。
第五步:向A试管的溶液中加入少量稀硫酸,再慢慢滴入过量的H2O2溶液,溶液的红色先变深,之后红色逐渐褪去。
红色变深的原因是(用离子方程式表示) 红色又逐渐褪去的原因可能是
设计实验证明你的推测
第六步:向B试管的溶液中加入一片VC,片刻后溶液红色也褪去,说明VC有 性。怎样理解药品说明书中所述“与VC(维生素C)同服可增加本品吸收”这句话?
。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com