
题目列表(包括答案和解析)

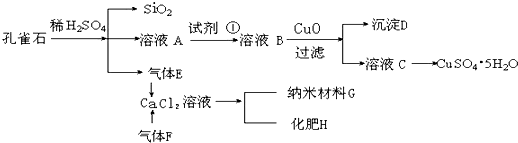

(16分)孔雀石主要含Cu2(OH)2CO3,还含少量Fe、Si的化合物,实验室以孔雀石为原料制备CuSO4·5H2O及CaCO3,步骤如下:
试回答下列问题:
(1)在未加入H2O2的溶液A中,存在的金属离子有Cu2+、Fe2+、Fe3+。若检验该溶液中Fe3+,选择最合适的试剂是 (填代号)。
A.KMnO4溶液 B.Fe粉 C. Na2CO3溶液 D.KSCN溶液
向溶液A中加入H2O2,H2O2在该反应中作氧化剂。实验室选用H2O2而不用Cl2作氧化剂。除考虑环保因素外,另一原因是不引入杂质 离子。
(2)由溶液C获得CuSO4·5H2O,需要经过加热浓缩, ,过滤等操作。除烧杯、漏斗外,过滤操作还需用到另一玻璃仪器,该仪器在此操作中的主要作用是 。
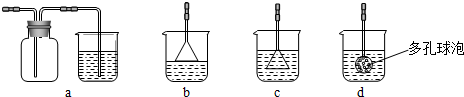
(3)制备CaCO3时,发生反应的化学方程式是 ;若实验过程中有氨气逸出,可选用下列装置中的 (填代号)装置吸收氨气。
(烧杯中的液体都为水)
(4)欲测定溶液A中Fe2+的浓度,需配制100 mL0.1 mol∕LKMnO4标准溶液。配制该溶液时:除烧杯、玻璃棒、胶头滴管外,还需的一种玻璃仪器是 ;当往该玻璃仪器中加蒸馏水至接近刻度线1-2cm时,应改用 滴加蒸馏水至溶液的凹液面正好与刻度线相平。
(12分)孔雀石主要含Cu2(OH)2CO3,还含少量Fe的氧化物和SiO2,实验室以孔雀石为原料制备CuSO4·5H2O及CaCO3,步骤如下: 
试回答下列问题:
(1)B物质的化学式是 在未加入H2O2的溶液中,存在的金属离子有Cu2+、Fe2+、Fe3+。若检验该溶液中Fe3+,选择最合适的试剂是 (填代号)。
| A.KMnO4溶液 | B.Fe粉 | C.Na2CO3溶液 | D.KSCN溶液 |
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com